题目内容
近年来研制的NF3气体可用作氟化氢—氟化氚高能化学激光器的氟源,也可作为火箭推进剂,NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2=NF3+3NH4F,下列说法中不正确的是( )
A.NF3的形成过程用电子式可表示为 |
| B.NF3分子空间构型为三角锥形 |
| C.NF3的氧化性大于F2 |
| D.NH4F中既有离子键又有极性共价键 |
C
解析试题分析:氮元素和氟元素均是活泼的非金属,二者形成的化学键是极性键,即NF3是含有共价键的共价化合物,A正确;NF3分子空间构型与氨气的类似,均是三角锥形结构,B正确;NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2=NF3+3NH4F,乙醇氟气的氧化性强于NF3的,选项C不正确;NH4F与氯化铵的结构是相似的,既有离子键又有极性共价键,选项D正确,答案选C。
考点:考查化学键、电子式、氧化性强弱比较
点评:该题以NF3为载体,重点考查学生的化学键、化合物的形成过程以及氧化还原反应的有关应用,有利于调动学生的学习兴趣,激发学生的学习积极性。根据与氨气、氯化铵的结构相似是答题的前提。

练习册系列答案
相关题目
下列说法与键能、键长无关的是
| A.H2O的沸点比H2S的高 | B.SiC的熔点比晶体硅的高 |
| C.O2比N2的化学性质更活泼 | D.HF比HCl稳定 |
下列说法正确的是
| A.离子化合物中一定含有金属元素 | B.构成分子晶体的微粒中一定含有共价键 |
| C.原子晶体熔化要破坏共价键 | D.只有离子化合物中才存在离子 |
下列情况会破坏共价键的是
| A.氯化纳加热融化 | B.氢氧化钠溶于水 |
| C.氯化氢气体溶于水 | D.酒精溶于水 |
下列说法正确的是
| A.全部由非金属元素组成的化合物一定是共价化合物 |
| B.含有共价键的化合物不一定是共价化合物 |
| C.由共价键形成的分子一定是共价化合物 |
| D.硫酸分子中有H+和SO42-两种离子 |
下列事实中,能够证明HCl是共价化合物的是
| A.HCl易溶于水 | B.液态的HCl不导电 |
| C.HCl不易分解 | D.HCl溶于水能电离,呈酸性 |
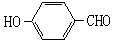 和
和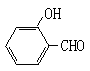 的沸点高低并说明理由_________。
的沸点高低并说明理由_________。