题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是:
A.1 L 0.1 mol·L-1亚硫酸钠溶液含有的SO32-数目为0.1NA
B.标准状况下,5.6L O2和O3的混合气体含有的氧原子数为0.5NA
C.向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,转移电子的总数为NA
D.30g甲醛中含共用电子对总数为4NA
【答案】D
【解析】
A选项,1 L 0.1 mol·L-1亚硫酸钠溶液物质的量为0.1mol,但亚硫酸是弱酸,电离出的SO32-数目小于0.1NA,故A错误;
B选项,标准状况下,5.6L O2和O3的混合气体即物质的量为0.25mol,如果全部是为氧气,则氧原子数为0.5 NA,如果全部是为臭氧,则氧原子数为0.75 NA,因此5.6L O2和O3的混合气体含有的氧原子数为0.5NA到0.75 NA之间,故B错误;
C选项,向FeI2溶液中通入适量Cl2,氯气先氧化I-,再氧化Fe2+,由于I-的物质的量未知,故此反应转移的电子数无法计算,故C错误;
D选项,30g甲醛物质的量为1 mol, 中含共用电子对总数为4NA,故D正确;
中含共用电子对总数为4NA,故D正确;
故答案为D。

 出彩同步大试卷系列答案
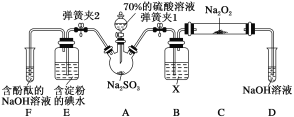
出彩同步大试卷系列答案【题目】资料显示“强酸性或强碱性溶液可使品红溶液褪色”。某兴趣小组探究SO2使品红溶液褪色的原因,实验如下。
Ⅰ.探究体现漂白性的主要微粒
实验一:将SO2分别通入0.1%品红水溶液和0.1%品红乙醇溶液中。观察到前者褪色而后者不褪色。
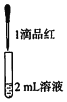
实验二:
| 试管中的液体 | 现象 |
a.0.1mol/L SO2溶液(pH=2) | 溶液逐渐变浅,约90s后完全褪色 | |
b.0.1mol/LNaHSO3溶液(pH=5) | 溶液立即变浅,约15s后完全褪色 | |
c.0.1mol/LNa2SO3溶液(pH=10) | 溶液立即褪色 | |
d.pH=10 NaOH溶液 | 红色溶液不变色 | |
e.pH=2 H2SO4溶液 | 红色溶液不变色 |
(1)SO2水溶液中含![]() 的微粒有___。
的微粒有___。
(2)解释NaHSO3溶液显酸性的原因是___。
(3)实验d的目的是___。
(4)由实验一、二可知:该实验条件下,SO2使品红溶液褪色时起主要作用的微粒是___。
Ⅱ.探究褪色过程的可逆性
甲同学:向a实验后的无色溶液中滴入NaOH溶液至pH=10时,溶液颜色不变。
乙同学:向a实验后的无色溶液中滴入Ba(OH)2溶液至pH=10时,生成白色沉淀,溶液变红。
(5)实验方案合理的是___(选填“甲”或“乙”)。结合离子方程式说明其原因是___。
(6)丙同学利用SO2的还原性设计并完成了下列实验:向a实验后的无色溶液中滴入过量___(填编号),使溶液最终恢复红色。也得出结论:该褪色过程是可逆的。
A.稀硝酸 B.氯水 C.双氧水