题目内容
5.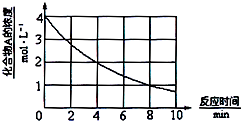 化合物A在一定条件下发生分解反应,反应物浓度随反应时间的变化如图所示.则化合物A在4~8min间的平均反应速率为( )
化合物A在一定条件下发生分解反应,反应物浓度随反应时间的变化如图所示.则化合物A在4~8min间的平均反应速率为( )| A. | 0.20mol•L-1•min-1 | B. | 0.25mol•L-1•min-1 | ||
| C. | 0.30mol•L-1•min-1 | D. | 0.50mol•L-1•min-1 |
分析 由图可知,4min时,化合物A的浓度为2mol/L,8min时A的物质的量浓度为1mol/L,根据v=$\frac{△c}{△t}$计算反应4~8min间的平均反应速率.
解答 解:由图可知,4~8 min期间,反应物浓度变化为(2-1)mol/L=1mol/L,所以4~8 min期间,反应速率为$\frac{1mol/L}{8min-4min}$=0.25 mol/(L•min);故选B.
点评 本题考查反应速率的有关计算,难度中等,根据图中浓度变化判断相同时间内的浓度变化量是解题关键.

练习册系列答案
相关题目
3.无色的有机物Ⅰ是印制防伪商标的一种原料,在紫外光辐射下Ⅰ可转变成结构Ⅱ(显橙色),反应如下(R1、R2、R3是烃基):有关上述变化的说法不正确的是( )
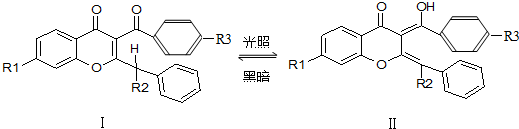

| A. | Ⅰ和Ⅱ互为同分异构体 | B. | Ⅱ可看作醇类 | ||
| C. | Ⅰ、Ⅱ均能发生加成反应 | D. | Ⅰ属于芳香烃 |
13.有机物的结构简式如图: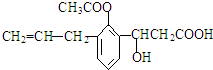 ,则此有机物可发生的反应类型有:( )①取代 ②加成 ③酯化 ④水解 ⑤氧化 ⑥中和.
,则此有机物可发生的反应类型有:( )①取代 ②加成 ③酯化 ④水解 ⑤氧化 ⑥中和.
 ,则此有机物可发生的反应类型有:( )①取代 ②加成 ③酯化 ④水解 ⑤氧化 ⑥中和.
,则此有机物可发生的反应类型有:( )①取代 ②加成 ③酯化 ④水解 ⑤氧化 ⑥中和.| A. | ①②④⑤⑥ | B. | ②③④⑤ | C. | ①②③④⑤⑥ | D. | ②③④⑤⑥ |
10.相同温度和压强下,在容积为2L的密闭容器中发生反应:2HI(g)?H2(g)+I2(g),达到平衡状态的标志是( )
| A. | c(H2)保持不变 | |
| B. | c(H2)=c(I2) | |
| C. | 2v正(HI)=v逆(I2) | |
| D. | 拆开2 mol H-I共价键,同时生成1 mol H-H共价键 |
17.关于液晶的叙述中,错误的是( )
| A. | 液晶是物质的一种聚集状态 | |
| B. | 液晶具有流动性 | |
| C. | 液晶和液态是物质的同一种聚集状态 | |
| D. | 液晶具有各向异性 |
14.下列有关物质的性质,说法正确的是( )
| A. | SiO2既能与氢氟酸反应,又能与烧碱反应,所以它是两性氧化物 | |
| B. | Cl2、SO2都能使紫色石蕊试液与品红溶液褪色 | |
| C. | 相同质量的Cu分别与过量的体积相同的浓硝酸、稀硝酸反应,反应中铜失去的电子数相等 | |
| D. | 32g Cu与50mL 18.4mol/L的硫酸溶液共热,充分反应后,被还原的H2SO4为0.46mol |
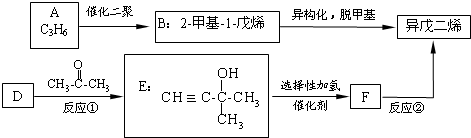
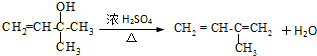
 某化工厂生产的某产品只含C、H、O三种元素,其分子模型如下图所示(图中球与球之间的连线代表化学键,如单键、双键等).
某化工厂生产的某产品只含C、H、O三种元素,其分子模型如下图所示(图中球与球之间的连线代表化学键,如单键、双键等). ,用1H核磁共振谱可以证明该化合物的核磁共振氢谱中有3种吸收峰.
,用1H核磁共振谱可以证明该化合物的核磁共振氢谱中有3种吸收峰. .
.
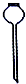


 .
. .
.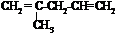 外,还有
外,还有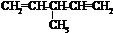 、
、 (填结构简式,已知
(填结构简式,已知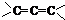 不稳定).
不稳定).