题目内容
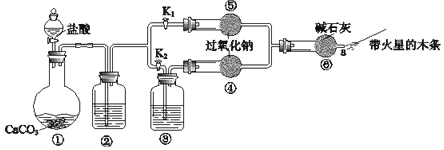
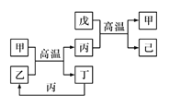
【题目】X、Y、Z、W是原子序数依次增大的前四周期元素,X、Z的周期序数=族序数,由这四种元素组成的单质或化合物存在如图所示的转化关系,其中甲、戊是两常见的金属单质,丁是非金属单质,其余为氧化物且丙为具有磁性的黑色晶体。下列说法正确的是
A. W的原子序数是Z的两倍,金属性强于Z
B. W元素在周期表中的位置是第四周期VIII族
C. 丙属于两性氧化物
D. 等物质的量的甲和戊完全溶于稀硝酸,消耗的HNO3的量一定相等
【答案】B
【解析】
X、Y、Z、W是原子序数依次增大的前四周期元素,X、Z的周期序数=族序数,则X是H元素,Z是Al元素;由这四种元素组成的单质或化合物存在如图所示转化关系,其中甲、戊是两常见的金属单质,丁是非金属单质,其余为氧化物且丙为具有磁性的黑色晶体,则丙是Fe3O4,结合元素及化合物的性质逆推可知甲为Fe,乙为H2O,丁是H2,戊为金属单质,可以与Fe3O4反应产生Fe单质,因此戊是Al单质,己为Al2O3,结合原子序数的关系可知Y是O元素,W是Fe元素,据此分析解答。
综上所述可知X是H元素,Y是O元素,Z是Al元素,W是Fe元素。甲是Fe单质,乙是H2O,丙是Fe3O4,丁是H2,戊是Al单质,己是Al2O3。
A.Fe原子序数是26,Al原子序数是13,26为13的2倍,金属性Al>Fe,A错误;
B.Fe是26号元素,在元素周期表中位于第四周期VIII族,B正确;
C.丙是Fe3O4,只能与酸反应产生盐和水,不能与碱发生反应,因此不是两性氧化物,C错误;
D.Fe是变价金属,与硝酸反应时,二者的相对物质的量的多少不同,反应失去电子数目不同,可能产生Fe2+,也可能产生Fe3+,而Al是+3价的金属,因此等物质的量的甲和戊完全溶于稀硝酸,消耗的HNO3的量不一定相等,D错误;
故合理选项是B。

【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | 85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________。
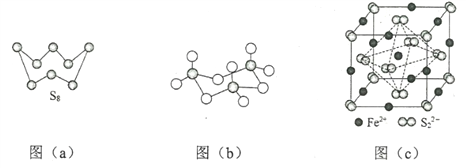
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为______nm。
所形成的正八面体的体心,该正八面体的边长为______nm。