题目内容
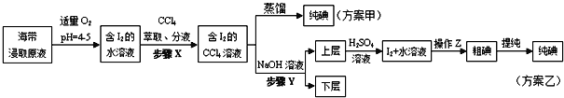
【题目】氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。

回答下列问题:
(1)检验滤液中的SO42-的方法是_______________________________________。
(2)试剂I的化学式为__________,加入过量试剂I后,①对应的实验操作是____,①中发生反应的离子方程式为___________________ 、__________________。
(3)试剂II的化学式为_________,②中加入过量试剂II的目的是_______________。
(4)试剂III的名称是________,操作③为__________、冷却结晶、过滤、洗涤、干燥,得到KCl晶体。
【答案】取少量滤液于试管中,先向其中加入盐酸酸化,再加入BaCl2溶液,若有白色沉淀生成,则有SO42-,反之则无; BaCl2; 过滤 Ba2++SO42-=BaSO4↓ Ba2++CO32-=BaCO3↓ K2CO3 除去多余的Ba2+ 盐酸 蒸发浓缩
【解析】
(1)首先在试液中加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42-;
(2)用氯化钡溶液,能同时除去硫酸根离子和碳酸根离子,根据离子方程式的书写规则书写;
(3)为除去过量的钡离子选用K2CO3作试剂,不仅能除去钡离子同时还生成氯化钾;
(4)试剂Ⅲ的名称是盐酸,操作③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到KCl晶体。
(1)首先在试液中加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42-,反之则无,故答案为:取少量滤液于试管中,先向其中加入盐酸酸化,再加入BaCl2溶液,若有白色沉淀生成,则有SO42-,反之则无;
(2)要除掉杂质离子硫酸根和碳酸根,应加入过量的氯化钡溶液,碳酸根和硫酸根生成不溶于水的钡盐,同时生成氯化钾,离子方程式为:SO42-+Ba2+=BaSO4↓,CO32-+Ba2+=BaCO3↓,
故答案为:BaCl2;过滤;Ba2++SO42-=BaSO4↓,Ba2++CO32-=BaCO3↓;
(3)要除掉多余的钡离子,要加入碳酸钾,碳酸钾和氯化钡反应生成碳酸钡沉淀同时生成氯化钾,离子方程式为CO32-+Ba2+=BaCO3↓,
故答案为:K2CO3;除去多余的Ba2+;
(4)要除掉多余的碳酸根,要滴加适量的盐酸,碳酸根离子和盐酸反应生成二氧化碳和水,离子方程式为CO32-+2H+=CO2↑+H2O,操作③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到KCl晶体。故答案为:盐酸;蒸发浓缩;

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案