题目内容
已知W、X、Y、Z四种短周期主族元素在周期表中的相对位置右图所示,下列有关说
法正确的是
A.Y的化学活泼性一定比W强
B.Y元素的原子半径可能比X元素的小
C.Z的气态氢化物的稳定性一定比X的强
D.Z的原子序数可能是X的原子序数的2倍
法正确的是
| W | X |
| Y | Z |
B.Y元素的原子半径可能比X元素的小
C.Z的气态氢化物的稳定性一定比X的强
D.Z的原子序数可能是X的原子序数的2倍
D
试题分析:根据元素周期律,Y和W同主族,Y的还原性比W强,但氧化性比W弱,故A选项错误;同周期主族元素半径从左往右依次减小,同主族从上到下依次增大,故Y元素半径一定比X元素的大,B选项错误;同主族元素从上到下气态氢化物的稳定性依次减弱,故Z的比X的弱,C选项错误;根据四种短周期元素的相对位置可知,W、X是第二周期因素,Y、Z是第三周期因素,若X、Z分别为氧元素和硫元素时,Z的原子序数是X的原子序数的2倍,故D选项正确。
点评:本题考查学生对元素周期律的掌握,分析此题时,应对元素周期表的“位构性”三者有较好的把握和理解。难度较小。

练习册系列答案
相关题目

 的物质。其转化关系如下图所示(图中某些生成物已略去),物质A与物质B之间的反应不在溶液中进行,通常状况下D为气体
的物质。其转化关系如下图所示(图中某些生成物已略去),物质A与物质B之间的反应不在溶液中进行,通常状况下D为气体

 1)若A、B、D均为短周期元素的单质,C为化合物且
1)若A、B、D均为短周期元素的单质,C为化合物且 气体D就是物质B,又知D气体不可燃,则B的分子式
气体D就是物质B,又知D气体不可燃,则B的分子式 是
是  在一定条件下E还可以和氧气发生反应。则A位于在周期表中的 周期 族。A和
在一定条件下E还可以和氧气发生反应。则A位于在周期表中的 周期 族。A和 B反应生成C的化学方程式是 。
B反应生成C的化学方程式是 。
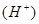 的能力由强到弱的顺序是 (用离子方程式加以说明)。
的能力由强到弱的顺序是 (用离子方程式加以说明)。