题目内容
【题目】对于可逆反应 N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,下列研究目的和示意图相符的是
2NH3(g) ΔH<0,下列研究目的和示意图相符的是
A | B | C | D | |
研究目的 | 压强对反应的影响(p2>p1) | 温度对平衡转化率的影响 | 平衡体系增加 N2的浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A.AB.BC.CD.D
【答案】C
【解析】
A.合成氨反应是气体体积缩小的反应,则利用压强对化学平衡及化学反应速率的影响分析;
B.合成氨的反应是放热反应,利用温度对化学平衡的影响及图象来分析;
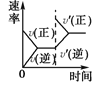
C.利用增大反应物的浓度对化学平衡移动的影响并结合图象来分析;
D.利用催化剂对化学反应速率及化学平衡的影响,结合图象来分析。
A.该反应的正反应是气体体积减小的反应,增大压强平衡向正反应方向移动,则氨气的体积分数增大,并且压强越大,化学反应速率越大,达到化学平衡的时间越少,与图象不符,A错误;
B.因该反应是放热反应,升高温度化学平衡向逆反应反应移动,则氮气的转化率降低,与图象中转化率增大不符,B错误;
C.反应平衡后,增大氮气的量,则这一瞬间正反应速率增大,逆反应速率不变,然后正反应速率在不断减小,逆反应速率不断增大,直到新的平衡,与图象符合,C正确;
D.因催化剂对化学平衡无影响,但催化剂加快化学反应速率,则有催化剂时达到化学平衡的时间少,与图象不符,D错误;
故合理选项是C。

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目