题目内容
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
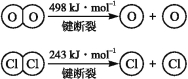
ⅱ.
(1)反应A的热化学方程式是 。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”) 。
【答案】(1)4HCl(g)+O2(g)2Cl2(g)+2H2O(g) ΔH=-115.6 kJ·mol-1 (2)32 强
【解析】
试题分析:由题给条件可知,4 mol HCl被氧化,放出热量为115.6 kJ,可知ΔH=-115.6 kJ·mol-1;由ΔH=-(生成物键能之和-反应物键能之和)可得,E(H—O)-E(H—Cl)= kJ·mol-1=31.9 kJ·mol-1,键能越大,化学键越稳定、越强,所以水中的H—O键比氯化氢中H—Cl键强。

练习册系列答案
相关题目
【题目】已知25℃时一些难溶物质的溶度积常数如下:
化学式 | Zn(OH)2 | ZnS | AgCl | Ag2S | MgCO3 | Mg(OH)2 |
溶度积 | 5×10-17 | 2.5×10-22 | 1.8×10-10 | 6.3×10-50 | 6.8×10-6 | 1.8×10-11 |
根据上表数据,判断下列化学方程式不正确的是
A. 2AgCl+Na2S═2NaCl+Ag2S
B. MgCO3+H2O![]() Mg(OH)2+CO2↑
Mg(OH)2+CO2↑
C. ZnS+2H2O═Zn(OH)2+H2S↑
D. Mg(HCO3)2+2Ca(OH)2═Mg(OH)2↓+2CaCO3↓+2H2O