题目内容
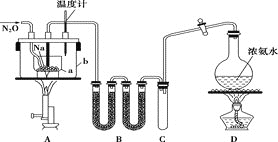
【题目】叠氮化钠(NaN3)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并与氨气充分反应后,停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
已知:I.NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
II.NaNH2熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为___;装置C的主要作用是___。
(2)步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为___。步骤③中最适宜的加热方式为____(填“水浴加热”,“油浴加热”)。
(3)N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是(填序号)___。

(4)生成NaN3的化学方程式为____。
(5)图中仪器a用的是铁质而不用玻璃,其主要原因是____。
(6)步骤④中用乙醚洗涤的主要目的是____。
【答案】碱石灰 冷凝分离出水 2Na+2NH3![]() 2NaNH2+H2 油浴加热 I、IV 2NaNH2+N2O
2NaNH2+H2 油浴加热 I、IV 2NaNH2+N2O![]() NaN3+H2O 反应过程中可能会产生NaOH腐蚀玻璃 减少晶体的损失,有利于产品快速干燥
NaN3+H2O 反应过程中可能会产生NaOH腐蚀玻璃 减少晶体的损失,有利于产品快速干燥
【解析】
(1)制备的氨气中含有大量的水用碱石灰干燥氨气;
(2)氨气与熔化的钠反应生成NaNH2,Na元素化合价上升,N化合价不变,则H的化合价下降生成氢气;
(3)反应时NH4NO3已经融化成液态,装置的选择应该注意不能让融化的NH4NO3流出来,并且为了使管底部最充分均匀被加热需要使试管倾斜;
(4)NaNH2和N2O反应生成NaN3和水;
(5)反应过程中生成的水,又会与钠反应生成NaOH腐蚀玻璃;
(6)NaN3不溶于乙醚,减少晶体的损失,有利于产品快速干燥。
(1)制备的氨气中含有大量的水,用B装置盛放碱石灰干燥氨气,用C装置冷凝分离出水因此,本题正确答案是:碱石灰;冷凝分离出水;
(2)氨气与熔化的钠反应生成NaNH2,Na元素化合价上升,N化合价不变,则H的化合价下降生成氢气,方程式为:2Na+2NH3![]() 2NaNH2+H2;水的沸点为100℃,不能达到反应控制的温度210-220℃,故用油浴加热。
2NaNH2+H2;水的沸点为100℃,不能达到反应控制的温度210-220℃,故用油浴加热。
(3)NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),反应时NH4NO3已经融化成液态,装置的选择应该注意不能让融化的NH4NO3流出来,并且为了使管底部最充分均匀被加热需要使试管倾斜,故选装置I、IV;
(4)NaNH2和N2O反应生成NaN3和水,化学方程式为:2NaNH2+N2O![]() NaN3+H2O;
NaN3+H2O;
(5)反应过程中生成的水,又会与钠反应生成NaOH腐蚀玻璃,因此,本题正确答案是:反应过程可能生成的NaOH能腐蚀玻璃;
(6)NaN3不溶于乙醚,减少晶体的损失,有利于产品快速干燥,因此,本题正确答案是:减少晶体的损失,有利于产品快速干燥。