题目内容
【题目】实验室制取乙烯并检验乙烯性质的装置如图. 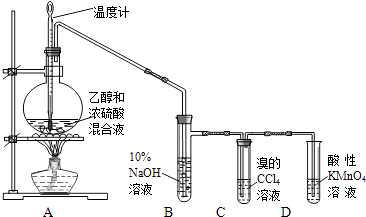
请回答有关问题:
(1)烧瓶中除反应物以外,还应放2﹣3块碎瓷片,目的是 .
(2)烧瓶中产生乙烯的反应方程式为 .
(3)反应开始后,可观察到C和D中共同的现象是;
C中的反应类型为反应、D中的反应类型为反应.
(4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是;10%的NaOH溶液起的作用是 .
【答案】
(1)防止暴沸
(2)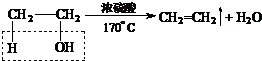
(3)褪色;加成;氧化
(4)浓硫酸将乙醇炭化,浓硫酸被碳还原产生了SO2;吸收挥发出的乙醇、乙酸和其它副产物气体(如乙醚、SO2和CO2等)
【解析】解:(1)反应条件是加热到170℃,因乙醇的沸点低,易暴沸,在圆底烧瓶中放2﹣3块碎瓷片的目的是防止暴沸,所以答案是:防止暴沸;
(2.)利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生消去反应,所以实验室制取乙烯的化学方程式为 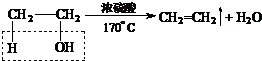 ,
,
所以答案是: 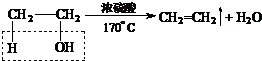 ;
;
(3.)乙烯含有碳碳双键,能和溴发生加成反应Br2+CH2=CH2→BrCH2CH2Br生成1,2﹣二溴乙烷褪色,乙烯被酸性高锰酸钾溶液氧化5CH2=CH2+12KMnO4+18H2SO4→10CO2+12MnSO4+28H2O+6K2SO4 , 导致高锰酸钾溶液褪色,所以答案是:褪色;加成;氧化;
(4.)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑是由于乙醇被浓硫酸氧化成碳,CH3CH2OH+4H2SO4(浓) ![]() 4SO2↑+CO2↑+7H2O+C;碳被浓硫酸氧化成二氧化碳,C+2H2SO4(浓)
4SO2↑+CO2↑+7H2O+C;碳被浓硫酸氧化成二氧化碳,C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O,且有强烈的刺激性气味气体为二氧化硫,因SO2+2NaOH=Na2SO3+H2O,CO2+2NaOH=Na2CO3+H2O,所以10%的NaOH溶液起的作用是吸收挥发出的乙醇其它副产物气体(如乙醚、SO2和CO2等)以防干扰检验乙烯性质实验,所以答案是:浓硫酸将乙醇炭化,浓硫酸被碳还原产生了SO2;吸收挥发出的乙醇和其它副产物气体(如乙醚、SO2和CO2等).
CO2↑+2SO2↑+2H2O,且有强烈的刺激性气味气体为二氧化硫,因SO2+2NaOH=Na2SO3+H2O,CO2+2NaOH=Na2CO3+H2O,所以10%的NaOH溶液起的作用是吸收挥发出的乙醇其它副产物气体(如乙醚、SO2和CO2等)以防干扰检验乙烯性质实验,所以答案是:浓硫酸将乙醇炭化,浓硫酸被碳还原产生了SO2;吸收挥发出的乙醇和其它副产物气体(如乙醚、SO2和CO2等).

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】2SO2(g)+ O2(g) ![]() 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断正确的是
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断正确的是
甲 | 乙 | 丙 | ||
起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
n(O2)/mol | 0.24 | 0.24 | 0.48 | |
SO2的平衡转化率/% | 80 | α1 | α2 |
A. 甲中反应的平衡常数小于乙
B. 该温度下,平衡常数值为400
C. 平衡时,丙中c(SO3)是甲中的2倍
D. 平衡时,甲中O2的转化率大于乙中O2的转化率