题目内容
13.下列物质除杂(括号内物质为杂质)的方法及试剂都正确的是( )| 物质 | 方法 | 试剂 | |
| A | 乙烷(乙烯) | 洗气 | 酸性高锰酸钾溶液 |
| B | AlCl3(MgCl2) | 过滤 | 氢氧化钠溶液 |
| C | CO2(SO2) | 洗气 | 饱和碳酸氢钠溶液 |
| D | Al(Mg) | 过滤 | 氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙烯被高锰酸钾氧化生成二氧化碳;
B.二者均与NaOH溶液反应;
C.二氧化碳与碳酸氢钠不反应,二氧化硫与碳酸氢钠反应生成二氧化碳;
D.Al与NaOH溶液反应.
解答 解:A.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应选溴水、洗气,故A错误;
B.二者均与NaOH溶液反应,将原物质除去,不能除杂,故B错误;
C.二氧化碳与碳酸氢钠不反应,二氧化硫与碳酸氢钠反应生成二氧化碳,则方法及试剂都正确,故C正确;
D.Al与NaOH溶液反应,将原物质除去,不能除杂,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、发生的反应为解答的关键,侧重分离提纯试剂及方法的考查,注意除杂的原则,题目难度不大.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案
相关题目
8.某同学按如图所示的装置进行实验.A、B为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处 SO42一从右向左移动.下列分析正确的是( )


| A. | 溶液中c(A2+)减小 | |
| B. | B的电极反应:B-2e-=B2+ | |
| C. | y电极上有H2产生,发生还原反应 | |
| D. | 反应初期,x电极周围出现白色胶状沉淀,一段时间以后沉淀逐渐溶解 |
4.下列实验描述,不正确的是( )
| A. | 同样是在氯气中点燃,铁少量生成的是氯化铁,过量时则生成氯化亚铁 | |
| B. | 同样是试纸检测,检验气体需要润湿,检验溶液时则一般不能润湿 | |
| C. | 同样是配制溶液,一定质量分数的溶液配制使用烧杯,而一定物质的量浓度的溶液配制则还需要容量瓶 | |
| D. | 同样是浓溶液(设其质量分数为ω )与水等体积混合,所得硫酸的浓度大于 0.5ω,氨水的则小于 0.5ω |
1.有四位同学分别对四种溶液中所含的离子进行检测,结果如下,其中错误的是( )
| A. | Ca2+、HCO3-、Cl-、K+ | B. | OH-、CO32-、Cl-、K+ | ||
| C. | Ba2+、Na+、OH-、NO3- | D. | Cu2+、NO3-、OH-、Cl- |
8.下列说法正确的是( )
| A. | 氯化钠和盐酸溶于水都发生电离,克服粒子间作用力的类型相同 | |
| B. | 氯化铵和水玻璃都属于离子化合物 | |
| C. | 直径介于1nm-10nm之间的微粒称为胶体 | |
| D. | 由IA族和VIA族元素可以形成含有原子个数比为l:1,离子个数比为2:l的离子化合物 |
5.下列关于化学反应的相关描述不正确的是( )
| A. | 胃舒平中含有氢氧化铝,可治疗胃酸过多:Al(OH)3+3HCl═AlCl3+3H2O | |
| B. | 碳铵是一种常用化肥,60℃分解完全:2NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O↑ | |
| C. | 生石灰可用作建筑材料:CaO+H2O=Ca(OH)2,属于化合反应 | |
| D. | 实验室常用氧化还原反应制备氧气:2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑ |
2.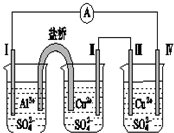 某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )
某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )
 某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )
某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )| A. | 电子方向:电极Ⅳ→→电极Ⅰ | B. | 电极Ⅰ发生还原反应 | ||
| C. | 电极Ⅱ逐渐溶解 | D. | 电极Ⅲ的电极反应:Cu-2e-═Cu2+. |
3.下列化学用语中,不正确的是( )
| A. | 钠离子结构示意图为: | |
| B. | 质子数为6,中子数为8的原子为:14C | |
| C. | H、D、T互为同位素 | |
| D. | 液态的氯气称为氯水 |