题目内容
【题目】能源危机是当前全球性的问题,“开源节流”是应对能源危机的重要举措。
(1)下列做法有助于能源“开源节流”的是________(填序号)。
A.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
B.大力开采煤、石油和天然气以满足人们日益增长的能源需求
C.开发太阳能、水能、风能、地热能等新能源,减少使用煤、石油等化石燃料
D.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,氧气充足时燃烧生成二氧化碳,反应中放出的热量如图所示。
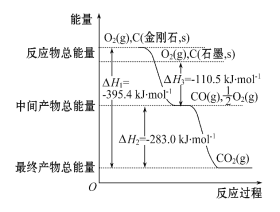
①在通常状况下,________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为ΔH= ____________。
②12 g石墨在24 g氧气中燃烧,生成气体36 g,该过程放出的热量为________。
(3)已知:N2、O2分子中化学键的键能分别是946 kJ·mol-1、497 kJ·mol-1。
N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ·mol-1。
NO分子中化学键的键能为________kJ·mol-1。
(4)综合上述有关信息,请写出CO和NO反应的热化学方程式:_________________________。
【答案】ACD 石墨 -393.5 kJ·mol-1 252.0 kJ 631.5 2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.0 kJ·mol-1
【解析】
(1)开源节流指的是开发新的能源,节约现有的化石能源;
A、大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源,开发了新的能源,能够节约化石燃料,A符合题意;
B、化石能源的使用会增加温室效应气体的排放,不利于环保和节约能源,B不符合题意;
C、开放新能源,减少化石能源的使用,C符合题意;
D、资源的重复使用,可以节约能源,D符合题意;
ACD符合题意;
(2) ①根据图示,石墨(s)+O2(g)的能量比金刚石(s)+O2(g)的能量低,则石墨的能量低于金刚石的能量;能量越低,越稳定,则石墨更稳定;根据图示,石墨的燃烧热为 △H3+△H4=-110.5kJ·mol-1+(-283. 0kJ·mol-1)=-393.5 kJ·mol-1;
②12g石墨完全燃烧生成CO2,需要32gO2,现只有24gO2,因此36g气体为CO和CO2的混合气体,设CO的物质的量为x,根据C守恒,CO2的物质的量为(1-x)mol,则根据质量守恒,有28x+44(1-x)=36,得x=0.5mol,则该石墨燃烧,生成了0.5molCO和0.5molCO2,生成0.5molCO,放出的热量为0.5×110.5kJ=55.25kJ;生成0.5molCO2,放出的热量为0.5×393.5kJ=196.75kJ;则总热量为55.25kJ+196.75kJ=252kJ;
(3)化学反应中,断开键需要吸热,形成键需要放热,假设NO分子中化学键的键能为E(NO),则有ΔH=946 kJ·mol-1+497 kJ·mol-1-2E(NO)= +180.0 kJ·mol-1,可得E(NO)= 631.5 kJ·mol-1;
(4)根据图示CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1(为反应①)
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1(为反应①)
N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ·mol-1(为反应②);
将(反应①×2-反应②)可得NO和CO的反应方程式,则ΔH =-283.0 kJ·mol-1×2-
(+180.0 kJ·mol-1)= -746.0 kJ·mol-1,,则CO和NO反应的热化学方程式为2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.0 kJ·mol-1。

【题目】某温度下,反应CO2(g)+H2(g)CO(g)+H2O(g)的平衡常数K=2.25,该温度下,在体积均为10L的三个密闭容器中分别加入反应物,起始加入量如表所示,下列判断不正确的是
起始量 | 甲 | 乙 | 丙 |
H2(mol) | 1 | 2 | 2 |
CO2(mol) | 1 | 1 | 2 |
A.反应开始时,甲中的反应速率最慢,丙中的反应速率最快
B.平衡时,甲和丙中CO2的转化率相等,均是60%
C.平衡时,乙中H2的转化率大于60%
D.平衡时,丙中c(H2)是0.08mol/L