题目内容
【题目】C1O2作为一种强氧化剂,是国际上公认的高效消毒灭菌剂,但因其易爆有毒,常用NaClO2替代。常温下,将NaOH固体加入到由0.1molC1O2溶于水配成的1L溶液中。溶液pH及部分组分含量变化曲线如图,下列叙述不正确的是

(已知:2C1O2+H2O![]() HC1O2+H++C1O3-)
HC1O2+H++C1O3-)
A. Ka(HClO2)≈10-4.5
B. 不能用pH试纸测该溶液的pH
C. 酸性:HClO2<HClO3,氧化性:HClO2>HClO3
D. 该图像上任何一点,都有c(C1O2-)+c(HC1O2)+c(C1O3-)=0.1mol·L-1
【答案】D
【解析】A项,HClO2的电离方程式为HClO2![]() H++ClO2-,HClO2的电离平衡常数Ka(HClO2)=
H++ClO2-,HClO2的电离平衡常数Ka(HClO2)=![]() ,根据图像当c(HClO2)=c(ClO2-)时溶液的pH
,根据图像当c(HClO2)=c(ClO2-)时溶液的pH![]() 4.5,Ka(HClO2)
4.5,Ka(HClO2)![]() 10-4.5,A项正确;B项,溶液中的ClO2、HClO2、ClO2-具有强氧化性,能使pH试纸褪色,不能用pH试纸测该溶液的pH,B项正确;C项,根据题给反应的离子方程式可见,HClO2为弱酸,HClO3为强酸,酸性:HClO2
10-4.5,A项正确;B项,溶液中的ClO2、HClO2、ClO2-具有强氧化性,能使pH试纸褪色,不能用pH试纸测该溶液的pH,B项正确;C项,根据题给反应的离子方程式可见,HClO2为弱酸,HClO3为强酸,酸性:HClO2![]() HClO3,一般同一元素不同氧化态的含氧酸中,低氧化态含氧酸的氧化性较强,氧化性:HClO2
HClO3,一般同一元素不同氧化态的含氧酸中,低氧化态含氧酸的氧化性较强,氧化性:HClO2![]() HClO3,C项正确;D项,根据2ClO2+H2O
HClO3,C项正确;D项,根据2ClO2+H2O![]() HClO2+H++ClO3-、HClO2
HClO2+H++ClO3-、HClO2![]() H++ClO2-,溶液中的物料守恒为c(ClO2)+c(HClO2)+c(ClO2-)+c(ClO3-)=0.1mol/L,D项错误;答案选D。
H++ClO2-,溶液中的物料守恒为c(ClO2)+c(HClO2)+c(ClO2-)+c(ClO3-)=0.1mol/L,D项错误;答案选D。

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案【题目】某课题组以硫铁矿烧渣(含 Fe2O3、 Fe3O4、 Al2O3、 CaO、 SiO2 等)为原料制取软磁用 Fe2O3(要求纯度>99.2%, CaO 含量<0.01%)。其工艺流程如下(所加入试剂均稍过量):
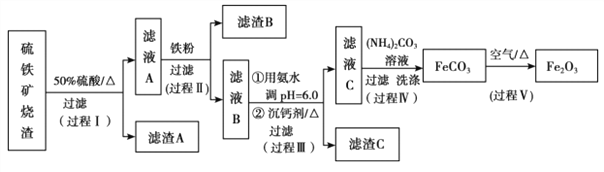
已知:生成氢氧化物的 pH 如下表所示
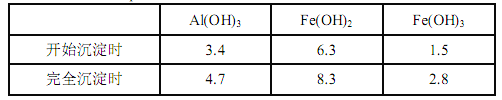
(1)滤渣 A 的主要成分是__________。
(2)在过程Ⅱ中可观察到产生少量气泡,溶液颜色慢慢变浅。能解释该实验现象的离子方程式有__________。
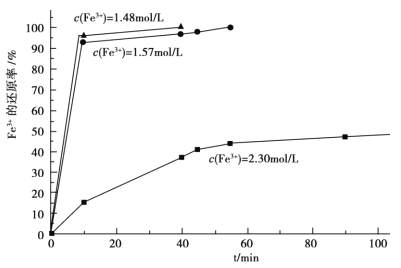
(3)在过程Ⅱ中,课题组对滤液 A 稀释不同倍数后,加入等质量的过量铁粉,得出 Fe3+浓度、还原率和反应时间的关系如图所示:结合上述实验结果说明:课题组选择稀释后c(Fe3+)为 1.60mol/L 左右的理由是______。
(4)在过程Ⅲ中,课题组在相同条件下,先选用了不同沉钙剂进行实验,实验数据见下表:(已知:滤液 B 中钙的含量以 CaO 计为 290—310mg/L)
沉钙剂 | Na2SO3 | H2C2O4 | (NH4)2CO3 | Na2CO3 | NH4F |
用量/g | 2 | 2 | 2 | 5 | 2 |
剩余CaO/mg/L) | 290 | 297 | 290 | 190 | 42 |
根据实验结果, 选择适宜的沉钙剂,得到滤渣 C 的主要成分有__________。
(5)在过程Ⅳ中,反应温度需要控制在 35℃以下,不宜过高,其可能的原因是__________。
(6)在过程Ⅴ中,反应的化学方程式是__________。