题目内容
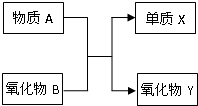 元素及其化合物的知识是“化学I”的重点内容. A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示:
元素及其化合物的知识是“化学I”的重点内容. A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示:试写出符合下列条件的化学方程式:
(1)若物质A为氧化物:
3CO+Fe2O3
3CO2+2Fe
| ||
3CO+Fe2O3
3CO2+2Fe
;
| ||
(2)若A为金属单质,B为金属氧化物:
2Al+Fe2O3
Fe+Al2O3
| ||
2Al+Fe2O3
Fe+Al2O3
;
| ||
(3)若A为金属单质,B为非金属氧化物:
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
;
| ||
(4)若A和X均为非金属单质:
2C+SiO2
Si+2CO↑
| ||
2C+SiO2
Si+2CO↑
;
| ||
(5)若A为非金属单质,X为金属单质:
H2+Cu
Cu+H2O
| ||
H2+Cu
Cu+H2O
.
| ||
分析:(1)A为氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,A、Y是同种元素的氧化物,且氧化物A作还原剂,中学常见的A为CO,据此书写;
(2)A为金属单质,B为金属氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,考虑铝热反应;
(3)若A为金属单质,B为非金属氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,中学常见为镁在二氧化碳中燃烧;
(4)若A和X均为非金属单质,由转化关系:A+氧化物B→单质X+氧化物Y,B、Y都为非金属氧化物,中学常见为碳与二氧化硅反应;
(5)若A为非金属单质,X为金属单质:可以是氢气还原氧化铜,或碳还原氧化铜;
(2)A为金属单质,B为金属氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,考虑铝热反应;
(3)若A为金属单质,B为非金属氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,中学常见为镁在二氧化碳中燃烧;
(4)若A和X均为非金属单质,由转化关系:A+氧化物B→单质X+氧化物Y,B、Y都为非金属氧化物,中学常见为碳与二氧化硅反应;
(5)若A为非金属单质,X为金属单质:可以是氢气还原氧化铜,或碳还原氧化铜;
解答:解:(1)A为氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,A、Y是同种元素的氧化物,且氧化物A作还原剂,中学常见的A为CO,
符合条件的方程式如:3CO+Fe2O3
3CO2+2Fe,故答案为:3CO+Fe2O3
3CO2+2Fe;
(2)A为金属单质,B为金属氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,考虑铝热反应,反应方程式如2Al+Fe2O3
2Fe+Al2O3,
故答案为:2Al+Fe2O3
2Fe+Al2O3;
(3)若A为金属单质,B为非金属氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,中学常见为镁在二氧化碳中燃烧,
反应方程式为:2Mg+CO2
2MgO+C,故答案为:2Mg+CO2
2MgO+C;
(4)若A和X均为非金属单质,由转化关系:A+氧化物B→单质X+氧化物Y,B、Y都为非金属氧化物,中学常见为碳与二氧化硅反应,
反应方程式为2C+SiO2
Si+2CO↑,故答案为:2C+SiO2
Si+2CO↑.
(5)若A为非金属单质,X为金属单质,A+氧化物B→单质X+氧化物Y,B为金属氧化物,Y都为非金属氧化物,中学常见为氢气还原氧化铜,反应的化学方程式为:H2+CuO
Cu+H2O;故答案为:H2+Cu
Cu+H2O;
符合条件的方程式如:3CO+Fe2O3
| ||
| ||
(2)A为金属单质,B为金属氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,考虑铝热反应,反应方程式如2Al+Fe2O3
| ||
故答案为:2Al+Fe2O3
| ||
(3)若A为金属单质,B为非金属氧化物,由转化关系:A+氧化物B→单质X+氧化物Y,中学常见为镁在二氧化碳中燃烧,
反应方程式为:2Mg+CO2
| ||
| ||
(4)若A和X均为非金属单质,由转化关系:A+氧化物B→单质X+氧化物Y,B、Y都为非金属氧化物,中学常见为碳与二氧化硅反应,
反应方程式为2C+SiO2
| ||
| ||
(5)若A为非金属单质,X为金属单质,A+氧化物B→单质X+氧化物Y,B为金属氧化物,Y都为非金属氧化物,中学常见为氢气还原氧化铜,反应的化学方程式为:H2+CuO
| ||
| ||
点评:本题考查元素化合物的推断,难度较大,关键是对化合物知识熟练掌握.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
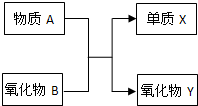 元素及其化合物的知识是“化学I”的重点内容. A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示:
元素及其化合物的知识是“化学I”的重点内容. A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示: