题目内容
7.(1)CuCl2溶液有时呈黄色,有时呈绿色或蓝色,这是因为有CuCl2的水溶液中存在如下平衡:[Cu(H2O)4]2++4Cl-?[CuCl4]2-+4H2O
蓝色 黄色
现欲使溶液由黄色变成蓝色,请写出一种可采用的方法:加入硝酸银溶液.
(2)在一定温度下,在一个容积不变的有催化剂的容器中,通入2moL N2和8moL H2.已知:N2(g)+3H2(g)?2NH3(g);△H=-92.2kJ/mol
达到平衡时容器内气体压强为起始时的80%.
①达到平衡时,N2的转化率为50%
②达到平衡时,容器内NH3的体积分数为25%
③达到平衡时,放出的热量b(填写序号)
a.小于92.2kJ b.等于92.2kJ b.大于92.2kJ d.以上三种情况皆有可能.
分析 (1)使溶液由黄色变成蓝色,应使平衡向左移动,可以加入硝酸银溶液降低氯离子浓度;
(2)在一定温度下,在一个容积不变的有催化剂的容器中,通入2moL N2和8moL H2,设转化氮气为xmol,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol):2 8 0
转化量(mol):x 3x 2x
平衡量(mol):2-x 8-3x 2x
达到平衡时容器内气体压强为起始时的80%,则10-2x=10×80%,解得x=1,据此解答.
解答 解:(1)使溶液由黄色变成蓝色,应使平衡向左移动,可以加入硝酸银溶液降低氯离子浓度,
故答案为:加入硝酸银溶液;
(2)在一定温度下,在一个容积不变的有催化剂的容器中,通入2moL N2和8moL H2,设转化氮气为xmol,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol):2 8 0
转化量(mol):x 3x 2x
平衡量(mol):2-x 8-3x 2x
达到平衡时容器内气体压强为起始时的80%,则10-2x=10×80%,解得x=1,
①达到平衡时,N2的转化率为$\frac{1mol}{2mol}$×100%=50%,故答案为:50%;
②达到平衡时,容器内NH3的体积分数为$\frac{2mol}{8mol}$×100%=25%,故答案为:25%;
③参加反应的n(N2)=1mol,所以放出的热量为1mol×92.2kJ•mol-1=92.2kJ,故选:b.
点评 本题考查化学平衡计算与影响因素,难度不大,注意三段式解题法在化学平衡计算中应用.

练习册系列答案
相关题目
11.当分散剂是水或其他液体时,分散质粒子的大小在1-100nm之间的分散系为( )
| A. | 胶体 | B. | 悬浊液 | C. | 乳浊液 | D. | 溶液 |
15.一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g)?2SO3(g).反应过程中测定的部分数据见下表(表中t1<t2),下列说法正确的是( )
| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 0.10 | 0.060 |
| t1 | 0.012 | |
| t2 | 0.016 |
| A. | 反应在0~t1 min内的平均速率为v(SO3)=0.088/t1 mol•L-1•min-1 | |
| B. | 保持其他条件不变,起始时向容器中充入0.10mol SO3和0.010mol O2,到达平衡时,n(SO2)=0.012mol | |
| C. | 保持其他条件不变,升高温度,平衡时c(SO2)=0.0070mol•L-1,则反应的△H>0 | |
| D. | 相同温度下,起始时向容器中充入0.050mol SO2和0.030mol O2,达到平衡时SO2转化率大于88% |
2.用 l-丁醇、溴化钠和过量较浓H2SO4混合物为原料,在实验室制备 1-溴丁烷,并检验反应的部分副产物.现设计如下装置,其中夹持仪器、加热仪器及冷却水管没有画出.
请根据实验步骤,回答下列问题:(已知:NaBr+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HBr)
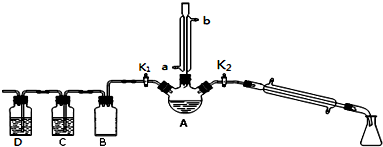
(1)关闭K1和K2,接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷.竖直冷凝管的作用 是冷凝回流,使冷水从a(填a或b)处流入.
(2)写出A中发生反应的主要化学方程式:NaBr+H2SO4═HBr+NaHSO4、HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O
(3)理论上,上述反应的生成物还可能有:丁醚、1-丁烯、溴化氢、硫酸氢钠、水等.熄灭A处酒 精灯,在竖直冷凝管上方塞上塞子、打开K1,利用余热继续反应直至冷却,通过C、D装置检验
部分副产物,C、D中应盛放的试剂分别是硝酸银、高锰酸钾溶液或溴水,
观察到D瓶中的现象是溶液褪色
(4)相关有机物的数据如下:
为了进一步精制1-溴丁烷,继续进行了如下实验:待烧瓶冷却后,拔去竖直的冷凝管,塞上带温度计的橡皮塞,关闭K1,打开K2,接通冷凝管的冷凝水,迅速升高温度至101.6℃,收集所得馏分就可以.
请根据实验步骤,回答下列问题:(已知:NaBr+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HBr)

(1)关闭K1和K2,接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷.竖直冷凝管的作用 是冷凝回流,使冷水从a(填a或b)处流入.
(2)写出A中发生反应的主要化学方程式:NaBr+H2SO4═HBr+NaHSO4、HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O
(3)理论上,上述反应的生成物还可能有:丁醚、1-丁烯、溴化氢、硫酸氢钠、水等.熄灭A处酒 精灯,在竖直冷凝管上方塞上塞子、打开K1,利用余热继续反应直至冷却,通过C、D装置检验
部分副产物,C、D中应盛放的试剂分别是硝酸银、高锰酸钾溶液或溴水,
观察到D瓶中的现象是溶液褪色
(4)相关有机物的数据如下:
| 物质 | 熔点/℃ | 沸点/℃ |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
19. 已知下列数据:
已知下列数据:
某学生在实验室制取乙酸乙酯的主要步骤如下:
①配制2mL浓硫酸、3mL乙醇(含18O)和2mL乙酸的混合溶液.
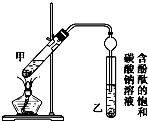
②按如图所示连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5min.
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置分层.
④分离出乙酸乙酯,洗涤、干燥.
(1)配制①中混合溶液的方法为应先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,最后加入冰醋酸;
反应中浓硫酸的作用是催化剂 吸水剂;写出制取乙酸乙酯的化学方程式:CH3COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O.
(2)上述实验中饱和碳酸钠溶液的作用是BC(填字母).
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇 C.减少乙酸乙酯的溶解 D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要理由是减少乙酸乙醇的挥发,减少副反应的发生;步骤③所观察到的现象是试管乙中的液体分成上下两层,上层无色,下层为红色液体,振荡后下层液体的红色变浅;
欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有分液漏斗;分离时,乙酸乙酯应从仪器上口倒(填“下口放”或“上口倒”)出.
(4)该同学反复实验,得出乙醇与乙酸的用量和得到的乙酸乙酯生成量如表:
表中数据x的范围是1.57<X<1.76;实验①②⑤探究的是增加乙醇或乙酸的用量对酯产量的影响.
 已知下列数据:
已知下列数据:| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.0 | 78.0 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
①配制2mL浓硫酸、3mL乙醇(含18O)和2mL乙酸的混合溶液.
②按如图所示连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5min.
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置分层.
④分离出乙酸乙酯,洗涤、干燥.
(1)配制①中混合溶液的方法为应先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,最后加入冰醋酸;
反应中浓硫酸的作用是催化剂 吸水剂;写出制取乙酸乙酯的化学方程式:CH3COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O.
(2)上述实验中饱和碳酸钠溶液的作用是BC(填字母).
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇 C.减少乙酸乙酯的溶解 D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要理由是减少乙酸乙醇的挥发,减少副反应的发生;步骤③所观察到的现象是试管乙中的液体分成上下两层,上层无色,下层为红色液体,振荡后下层液体的红色变浅;
欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有分液漏斗;分离时,乙酸乙酯应从仪器上口倒(填“下口放”或“上口倒”)出.
(4)该同学反复实验,得出乙醇与乙酸的用量和得到的乙酸乙酯生成量如表:
| 实验 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| ① | 2 | 2 | 1.33 |
| ② | 3 | 2 | 1.57 |
| ③ | 4 | 2 | x |
| ④ | 5 | 2 | 1.76 |
| ⑤ | 2 | 3 | 1.55 |
16. 用甲烷和二氧化碳可以制备化工原料.
用甲烷和二氧化碳可以制备化工原料.
(1)一定温度下,向容积恒为2L的密闭容器中通入3mol CO2,3mol CH4,发生如下反应:
CO2(g)+CH4(g)?2CO(g)+2H2(g)
反应在2min末达到平衡状态,此时测得CO2和CO的体积分数相等.清回答下列问题:
①2min内,用H2来表示的反应速率v(H2)=0.5mol/(L•min);
②此温度下该反应的平衡常数K=1;
③下列叙述可以作为该反应达到平衡状态的标志的是BC;(填选项字母)
A.v正(CH4)=v逆(H2)
B.容器内压强保持恒定不变
C.反应中断裂2mol C-H键同时消耗1mol H2
D.容器内混合气体的密度保持恒定不变
④已知:
则反应CO2(g)+CH4(g)?2CO(g)+2H2(g)△H=248kJ/mol.
⑤为提高CH4的转化率,可以采取的措施是减小反应压强、增大CO2的浓度.(写两点)
(2)在催化作用下,甲烷和二氧化碳还可以直接转化成乙酸.
①在不同温度下乙酸的生成速率如图所示:
在250-400℃范围内,乙酸的生成速率随温度变化的原因是温度超过250℃时,催化剂的催化效率降低.
②250℃与400℃时乙酸的生成速率相近,清分析判断实际生产选择的最佳温度是250℃.
 用甲烷和二氧化碳可以制备化工原料.
用甲烷和二氧化碳可以制备化工原料.(1)一定温度下,向容积恒为2L的密闭容器中通入3mol CO2,3mol CH4,发生如下反应:
CO2(g)+CH4(g)?2CO(g)+2H2(g)
反应在2min末达到平衡状态,此时测得CO2和CO的体积分数相等.清回答下列问题:
①2min内,用H2来表示的反应速率v(H2)=0.5mol/(L•min);
②此温度下该反应的平衡常数K=1;
③下列叙述可以作为该反应达到平衡状态的标志的是BC;(填选项字母)
A.v正(CH4)=v逆(H2)
B.容器内压强保持恒定不变
C.反应中断裂2mol C-H键同时消耗1mol H2
D.容器内混合气体的密度保持恒定不变
④已知:
| 物质 | H2 | CO | CH4 | CH3COOH |
| 燃烧热(kJ/mol) | 286 | 283 | 890 | 874 |
⑤为提高CH4的转化率,可以采取的措施是减小反应压强、增大CO2的浓度.(写两点)
(2)在催化作用下,甲烷和二氧化碳还可以直接转化成乙酸.
①在不同温度下乙酸的生成速率如图所示:
在250-400℃范围内,乙酸的生成速率随温度变化的原因是温度超过250℃时,催化剂的催化效率降低.
②250℃与400℃时乙酸的生成速率相近,清分析判断实际生产选择的最佳温度是250℃.