题目内容
常温下,物质的量浓度相等的下列物质的水溶液,pH最小的是
A. NaOH B. FeCl3 C. Na2CO3 D. NaCl
钠及其化合物具有广泛的用途。
(1)工业上制备金属钠的常用方法是_______。试写出制备金属钠的化学方程式_____________。金属钠可用于________________(写出Na在熔点低方面的一种用途)。
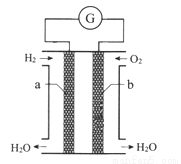
(2)用Na2CO3熔融盐作电解质,CO、O2、CO2为原料可组成新型电池。该电池的结构如图所示:

①正极的电极反应式为_______,电池工作时物质A可循环使用,A物质的化学式为_______。
②请写出检验Na2CO3中钠元素的方法_________________________。
(3)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 11.6 | 10.3 | 11.1 |
上述盐溶液的阴离子中,结合H+能力最强的是_________,根据表中数据,浓度均为0.01 mol·L-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是_______(填序号)。
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯。
①常温下,当300 mL 1 mol·L-1的NaOH溶液吸收4.48 L(折算成标准状况)SO2时,所得溶液pH>7,则溶液中各离子浓度由大到小的顺序为_______。
②已知几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加某浓度的NaOH溶液时,_______(填离子符号)先沉淀,Ksp_______Ksp(填“>”、“=”或“<”)。
X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如下图所示:
X | Y | |
Z | W |
请回答下列问题:
(1)W位于周期表中第__________周期,第____族;
(2)X可形成双原子分子,其分子的电子式是_____;Y和氢元素形成的10电子微粒中常见+1价阳离子为_____(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子为______;
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式______________________。
(4)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡时有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式是_____________。


 C B. 溴化铵的电子式:
C B. 溴化铵的电子式:
 D. 2-丙醇的结构简式:
D. 2-丙醇的结构简式: