题目内容
某温度下,将2 mol A和3 mol B充入一密闭的容器中,发生反应:
xA(g)+B(g) C(g)+D(g),5 min后达到平衡。已知各物质的平衡浓度关系为
C(g)+D(g),5 min后达到平衡。已知各物质的平衡浓度关系为
cx(A)·c(B)=c(C)·c(D),若在温度不变的情况下将容器的体积扩大为原来的10倍,
A的转化率不发生变化,则B的转化率为( )
A. 40% B. 60% C. 24% D. 4%
xA(g)+B(g)
 C(g)+D(g),5 min后达到平衡。已知各物质的平衡浓度关系为
C(g)+D(g),5 min后达到平衡。已知各物质的平衡浓度关系为cx(A)·c(B)=c(C)·c(D),若在温度不变的情况下将容器的体积扩大为原来的10倍,
A的转化率不发生变化,则B的转化率为( )
A. 40% B. 60% C. 24% D. 4%
A
试题分析:在温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,说明了压强的变化并不会影响该反应,所以该反应是反应前后分子数变的反应,故x为1,所以该反应为A(g)+B(g)
 C(g)+D(g),根据平衡常数K=c(A)·c(B)/(c(C)·c(D))=1,设该容器为1L,则反应的物质的量为a,则可以得到,(2-a)(3-a)/(a×a)=1,解答a=1.2,所以B的转化率="1.2/3=" 40% ,故本题的答案选择A。
C(g)+D(g),根据平衡常数K=c(A)·c(B)/(c(C)·c(D))=1,设该容器为1L,则反应的物质的量为a,则可以得到,(2-a)(3-a)/(a×a)=1,解答a=1.2,所以B的转化率="1.2/3=" 40% ,故本题的答案选择A。点评:本题考查了转化率的计算,该考点是高考常考的考点,本题要抓住的是在温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,说明了压强的变化并不会影响该反应,所以该反应是反应前后分子数变的反应,故x为1,然后根据K进行计算,该题难度中等。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
 C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大。请回答下列问题:
C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大。请回答下列问题: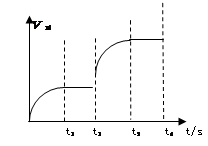
 zC达到平衡:
zC达到平衡: 2NH3 △H=-92.4 kJ·mol-1下图是该反应的速率—时间图像,一定条件下,t1时建立平衡, t2时改变某一条件,t3时又建立新平衡,t2时改变的条件可能是
2NH3 △H=-92.4 kJ·mol-1下图是该反应的速率—时间图像,一定条件下,t1时建立平衡, t2时改变某一条件,t3时又建立新平衡,t2时改变的条件可能是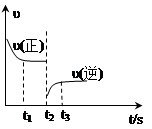
 2Z(g)在不同温度和压强下的产物Z的物质的量和反应时
2Z(g)在不同温度和压强下的产物Z的物质的量和反应时
 CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1,在800℃时的化学平衡常数K=1.0 。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1,在800℃时的化学平衡常数K=1.0 。某时刻测得该温度下的密闭容器中各物质的物质的量见下表: CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表: pC(g)已经达到平衡状态。已知n+m>p,正反应为放热反应。下列分析结论中正确的是( )
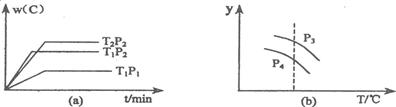
pC(g)已经达到平衡状态。已知n+m>p,正反应为放热反应。下列分析结论中正确的是( ) xC(g)符合下图(a)所示的关系(W(C)表示C的体积分数),由此推断关于图(b)的说法正确的是
xC(g)符合下图(a)所示的关系(W(C)表示C的体积分数),由此推断关于图(b)的说法正确的是