题目内容
19.氯元素的天然同位素有${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl.氯元素的相对原子质量为35.45,则天然氯元素中${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl的原子数目之比约为( )| A. | 3:1 | B. | 1:3 | C. | 3:2 | D. | 4:1 |
分析 氯元素的平均相对分子质量是由同位素的丰度计算出来的,同位素在自然界中的丰度,又称天然存在比,指的是该同位素在这种元素的所有天然同位素中所占的比例.
解答 解:设天然氯元素中35Cl 和37Cl的原子数目分别为x和y,依据题意有:$\frac{35×x+37×y}{x+y}$=35.45,解x:y≈3:1,
故选A.
点评 本题考查物质的量及相对分子质量的计算,熟悉摩尔质量与相对分子之间的关系即可解答,题目较简单.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
7.下列反应中一定有白色沉淀生成的是( )
| A. | 将久置的亚硫酸钠溶液中加入氯化钡溶液再加入稀盐酸 | |
| B. | 向碳酸钠溶液中加入酸性氯化钙溶液 | |
| C. | 向亚硫酸钠溶液中通入氯气再加入氯化钡和稀盐酸 | |
| D. | 向亚硫酸钠溶液中加入稀硝酸后再加入氯化钡溶液 | |
| E. | 二氧化硫通入氯化钡溶液中 |
4.下列实验“操作和现象”与“结论”对应关系正确的是( )
| 选项 | 操作和现象 | 结论 |
| A | CH4和Cl2混合于试管中光照,颜色逐渐褪去 | 二者发生了化合反应 |
| B | 向淀粉溶液中加入20%的硫酸,加热几分钟,冷却后再加入银氨溶液,水浴,没有银镜生成 | 淀粉没发生水解 |
| C | 将乙醇与浓硫酸共热产生气体直接通入酸性KMnO4溶液 | 检验乙烯的生成 |
| D | 向AgCl沉淀中滴加少量KI溶液,观察到白色沉淀转化为黄色沉淀 | 验证Ksp(AgCl)>Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
11.已知:H+H→H2 过程放出437.6kJ热量,下列说法正确的是( )
| A. | 氢气分子内每个氢原子都达到8电子稳定结构 | |
| B. | 相同条件下1mol H2的能量比2mol H的能量低 | |
| C. | 1mol H2离解成2mol H要放出437.6kJ热量 | |
| D. | 氢原子比氢分子性质更稳定 |
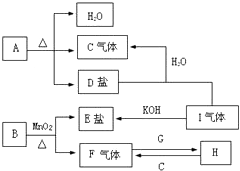 已知A、B、C、D、E、F、G、H、I九种物质,A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G是一种单质,I是一种化合物,H是一种淡黄色固体,它们的转化关系如图所示.请回答下列问题:
已知A、B、C、D、E、F、G、H、I九种物质,A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G是一种单质,I是一种化合物,H是一种淡黄色固体,它们的转化关系如图所示.请回答下列问题: