题目内容
TPE及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。TPE的结构简式如图,下列关于TPE的说法正确的是

A. TPE属于苯的同系物
B. TPE能发生加成反应,但不能取代反应
C. TPE与化合物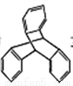 互为同分异构体
互为同分异构体
D. TPE的一氯代物有3种
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案一氧化碳是一种用途相当广泛的化工基础原料。
⑴.利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍。
Ni(s)+4CO(g) Ni(CO)4(g)该反应的ΔH_______0(选填“>”或“=”或“<”)。
Ni(CO)4(g)该反应的ΔH_______0(选填“>”或“=”或“<”)。
⑵.在高温下一氧化碳可将二氧化硫还原为单质硫。已知:
C(s)+O2(g)=CO2(g);ΔH1=-393.5 kJ·mol-1
CO2(g)+C(s)=2CO(g);ΔH2=+172.5 kJ·mol-1
S(s)+O2(g)=SO2(g);ΔH3=-296.0 kJ·mol-1
则2CO(g)+SO2(g)=S(s)+2CO2(g) ΔH4=________。
⑶.工业上一般采用CO与H2反应合成可再生能源甲醇,反应如下:
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测
得c(CO)=0.2mol·L-1,则CO的转化率为___________。
合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,通过反应进行甲醇合成,T1℃下此反应的平衡常数为160。此温度下,在密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
物质 | H2 | CO | CH3OH |
浓度/(mol·L-1) | 0.2 | 0.1 | 0.4 |
比较此时正、逆反应速率的大小:v正_______v逆 (填“>”、“<”或“=”);若其他条件不变,在T2℃反应10min后达到平衡,c(H2)=0.4 mol·L-1,则该时间内反应速率:v(CH3OH)=__________;
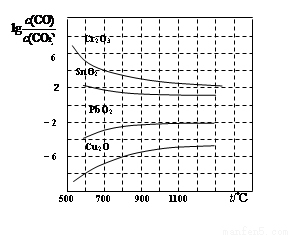
(4)金属氧化物被一氧化碳还原生成金属单质和二氧化碳。下图是四种金属氧化物被一氧化碳还原时lg[c(CO)/c(CO2)]与温度(t)的关系曲线图。800℃时,其中最易被还原的金属氧化物是____(填化学式),该反应的平衡常数数值(K)等于____________。
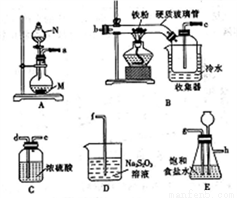
下列装置应用于实验室制NO并回收硝酸铜的实验,能达到实验目的是( )
A. 用装置制取NO 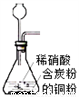 B. 用装置收集NO
B. 用装置收集NO 
C. 用装置分离炭粉和硝酸铜溶液 D. 用装置蒸干硝酸铜溶液制Cu(NO3)2•3H2O
D. 用装置蒸干硝酸铜溶液制Cu(NO3)2•3H2O 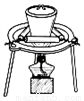
化学在日常生活中有着广泛的应用,下列对应项不存在因果关系的是
物质性质 | 实际应用 | |
A | 硅胶吸水能力强 | 食品、药品干燥剂 |
B | 油脂在碱性条件下水解 | 制肥皂 |
C | SiO2是酸性氧化物 | 光导纤维 |
D | Na2O2与CO2、H2O反应 | 潜水艇中作为氧气来源 |
A. A B. B C. C D. D




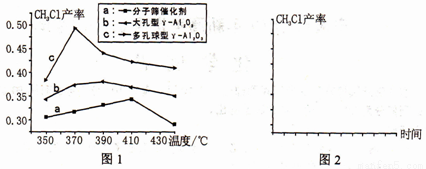
 CH3Cl(g)+H2O(g) △H=-31.9kJ·mol-1
CH3Cl(g)+H2O(g) △H=-31.9kJ·mol-1