题目内容
设NA为阿伏加德罗常数,下列说法中正确的是
| A.O2和O3的混合气体共6.4g,其中所含氧原子数一定为0.4NA |
| B.将标准状况下22.4LNO与11.2LO2混合后的体积约为22.4L |
| C.在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4molCl2转移的电子数为8NA |
| D.标准状况下11.2LCl2溶于1L水中,转移电子的数目为0.5NA |
A
解析试题分析:A、氧气和臭氧都是由氧原子构成的。因此在该题中的氧原子的物质的量为氧气和臭氧的总质量除以氧原子的摩尔质量,为0.4mol,所以正确;B、将标准状况下22.4LNO与11.2LO2混合后若完全反应生成二氧化氮,体积约为22.4L,但是二氧化氮与四氧化二氮之间存在一个转化平衡,所以生成的气体的总体积小于22.4L,错误;C、每生成4molCl2转移的电子数为7NA,错误;D、氯气与水的反应是一个可逆反应,不可以完全转化为盐酸和次氯酸,错误。
考点:考查物质的组成,平衡的存在,氧化还原反应。

练习册系列答案
相关题目
NA表示阿伏伽德罗常数的值,下列叙述错误的是
| A.2gD216O中含有的质子数、中子数、电子数均为NA |
| B.80g CuO和Cu2S的混合物含有铜原子数一定为NA |
| C.标准状况下,5.6L O2作氧化剂时转移电子数一定为NA |
| D.500mL 2mol·L-1Na2CO3溶液中含C微粒总数一定为NA |
用NA表示阿伏加德罗常数。下列说法正确的是
| A.12 g NaHSO4固体中含有的离子数为0.3 NA |
| B.足量Cl2与5.6 g Fe完全反应时,转移的电子数为0.2 NA |
| C.标准状况下,0.56 L 丙烷中含有的共价键数为0.25 NA |
| D.电解精炼铜时每转移NA个电子,阳极溶解32 g铜 |
设NA表示阿伏加德罗常数的值。下列说法正确的是 ( )
| A.标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.2 NA |
| B.常温常压下, 18 g H2O中含的质子数为10 NA |
| C.标准状况下,11.2 L CH2Cl2中含有的分子数目为0.5 NA |
| D.常温常压下, 2.24 L CO和CO2混合气体中含有的碳原子数目为0.1 NA |
NA为阿伏加德罗常数,下列叙述正确的是
| A.14 gC2H4和C3H6的混合气体中含有的原子数为3NA |
| B.25 ℃时,1 L pH=13的氢氧化钡溶液中含有0.2NA个氢氧根离子 |
| C.5.6克铁与一定量稀硝酸完全反应,电子转移数目一定为0.3NA |
| D.1.0L1mol/L的NaOH水溶液中含有的氧原子数目为2 NA |
NA表示阿伏加德罗常数,下列叙述正确的是
| A.6.4 g铜粉与足量硫粉充分反应,失去的电子数为0.2 NA |
| B.Na2O2与足量H2O反应生成0.2molO2,转移电子的数目为0.4 NA |
| C.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2 NA |
| D.0.5 mol·L-1CuCl2溶液中含有Cu2+数小于0.5 NA |
下列化学用语正确的是( )
A.聚丙烯的结构简式: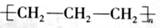 |
B.丙烷分子的比例模型: |
C.四氯化碳分子的电子式: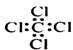 |
D.2-乙基-1,3-丁二烯分子的键线式: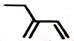 |
下列化学用语或模型正确的是( )
A.氯化氢的电子式: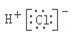 | B.N2的结构式:N≡N |
C.硫离子结构示意图: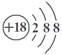 | D.CH4分子的球棍模型: |