题目内容
根据价层电子对互斥理论及原子的杂化理论判断NF3分子的空间构型和中心原子的杂化方式为
| A.直线形 sp杂化 | B.三角形 sp2杂化 |
| C.三角锥形 sp2杂化 | D.三角锥形 sp3杂化 |
D
试题分析:根据价层电子对互斥理论可知,氨气分子中氮原子含有的孤对电子对数=(5-3×1)÷2=1,所以氨气是三角锥形结构,氮原子是sp3杂化,答案选D。
点评:该题是高考中的常见题型,属于基础性试题的考查,主要是考查学生灵活运用价层电子对互斥理论判断分子空间构型的熟悉了解程度,旨在培养学生灵活运用基础知识解决实际问题的能力。

练习册系列答案
相关题目
 中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是
中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是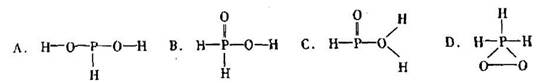
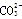 是等电子体,均为平面正三角形结构
是等电子体,均为平面正三角形结构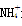 是等电子体,键角均为60°
是等电子体,键角均为60° 的化合物N5AsF6,下列叙述错误的是
的化合物N5AsF6,下列叙述错误的是