题目内容
【题目】某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验:
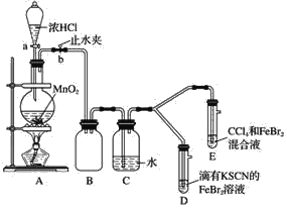
(1)①装置A中发生反应的离子方程式是______________。
②整套实验装置存在一处明显的不足,请指出_______________________。
(2)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化。D装置中:红色慢慢褪去。E装置中:CCl4层先由无色变为橙色,后颜色逐渐加深,直至变成红色。
为探究上述实验现象的本质,小组同学查得资料如下:

①用平衡移动原理(结合上述资料)解释Cl2过量时D中溶液红色褪去的原因___________,现设计简单实验证明上述解释:取少量褪色后的溶液,滴加____________溶液,若溶液颜色________,则上述解释是合理的。
②探究E中颜色变化的原因,设计实验如下:用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生。请结合上述资料用两步方程式(离子或化学方程式不限定)解释仅产生白色沉淀原因_________________________。
【答案】MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 缺少尾气处理装置 过量氯气和SCN-反应2SCN-+Cl2==2Cl-+(SCN)2,使SCN-浓度减小,则Fe3++3SCN-Fe(SCN)3平衡逆向移动而褪色 KSCN 变红色(或 FeCl3溶液,不变红) BrCl+H2O==HBrO+HCl、Ag++Cl-==AgCl↓
Mn2++Cl2↑+2H2O 缺少尾气处理装置 过量氯气和SCN-反应2SCN-+Cl2==2Cl-+(SCN)2,使SCN-浓度减小,则Fe3++3SCN-Fe(SCN)3平衡逆向移动而褪色 KSCN 变红色(或 FeCl3溶液,不变红) BrCl+H2O==HBrO+HCl、Ag++Cl-==AgCl↓
【解析】
打开活塞a,向圆底烧瓶中滴入适量浓盐酸,然后关闭活塞a,点燃酒精灯,会发现:D装置中:溶液变红,说明发生反应:Cl2+2Fe2+==2Cl-+2Fe3+,Fe3+与SCN-溶液反应生成Fe(SCN)3为红色;E装置中:通入少量氯气时,发生Cl2+2Br-===2Cl-+Br2。
(1)①在装置A中浓盐酸与MnO2在加热时发生反应产生氯气,发生反应的离子方程式是MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
②氯气是有毒气体,会造成大气污染,在整套实验装置存在一处明显的不足,就是缺少尾气处理装置。
(2)①Fe3++3SCN-Fe(SCN)3是一个可逆反应,当Cl2过量时,过量的氯气和SCN-反应2SCN-+Cl2===2Cl-+(SCN)2,使SCN-浓度减小,则Fe3++3SCN-Fe(SCN)3平衡逆向移动而褪色。
设计简单实验证明上述解释:取少量褪色后的溶液,滴加KSCN溶液,若溶液颜色变红色,就证明是平衡发生了移动;或向溶液中滴加FeCl3溶液,溶液不变红色,也证明溶液中SCN-浓度减小,平衡发生了移动;
②探究E中颜色变化的原因,用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生。这是由于Cl2+Br2==2BrCl;BrCl +H2O ==HBrO+HCl,Ag++Cl-===AgCl↓,所以溶液颜色变成红色。

 名校课堂系列答案
名校课堂系列答案【题目】(1)乙醇常被用做饮料的添加剂,在一定的条件下能被氧化为乙醛,乙醇___(“能”或“不能”)使酸性KMnO4溶液褪色;已知常温下,2.3g乙醇和一定量的氧气混合后点燃,恰好完全燃烧,放出68.35kJ热量,则该反应的热化学方程式为___。
(2)已知:
化学键 | Si—Cl | H—H | H—Cl | Si—Si |
键能/kJ·mol-1 | 360 | 436 | 431 | 176 |
且硅晶体中每个硅原子和其他4个硅原子形成4个共价键,工业上制取高纯硅的反应方程式为:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g),该反应的反应热为___kJ·mol-1。
Si(s)+4HCl(g),该反应的反应热为___kJ·mol-1。
(3)已知水的比热容为4.18×10-3kJ·g-1·C-1。10g硫黄在O2中完全燃烧生成气态SO2,放出的热量能使500 g H2O的温度由18℃升至62.4℃,则硫黄的燃烧热为____,热化学方程式为____。
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,可由NO与Cl2在常温常压下反应得到。ClNO 部分性质如下:黄色气体,熔点:-59.6℃,沸点:-6.4℃,遇水易水解。某研究性学习小组根据亚硝酰氯(ClNO)性质拟在通风橱中制取亚硝酰氯,设计了如下实验装置。、
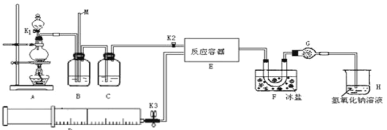
试回答下列问题:
(1)写出实验室利用装置A制备Cl2的离子反应方程式__________。
(2)装置B的作用是 ①__________,②____________。
(3)若用A装置制取NO气体,B中应该盛放_________。
(4)为使NO和Cl2恰好完全反应生成ClNO,理论上向E中通入NO和Cl2两种气体的流速比为___。
(5) 简述检查A、B、C所组成的实验装置气密性的操作_________。
(6)装置H吸收尾气,有同学认为尾气中的某种气体不能完全被吸收。为了充分吸收尾气,可将尾气与________________同时通入NaOH溶液中。
(7)已知:ClNO与H2O反应生成HNO2和HCl。
①设计实验证明 HNO2是弱酸:____________。(仅提供的试剂:1 molL-1HCl、 1 molL-1HNO2溶液、 NaNO2溶液、红色石蕊试纸、蓝色石蕊试纸)。
②通过以下实验测定ClNO样品的纯度。取F中所得液体3.0 g 溶于水,配制成250 mL 溶液;取出25.00 mL样品溶于锥形瓶中,用0.20 molL-1 AgNO3标准溶液滴定至终点,根据表中所给信息,应选用____________做指示剂,滴定终点的现象是______。
物质 | Ag2CrO4 | AgCl | AgI | Ag2S |
颜色 | 砖红色 | 白色 | 黄色 | 黑色 |
Ksp | 1×10-12 | 1.56×10-10 | 8.3×10-17 | 6.3 ×10-50 |
消耗标准AgNO3溶液的体积为20.00ml,亚硝酰氯(ClNO)的质量分数为________。