题目内容
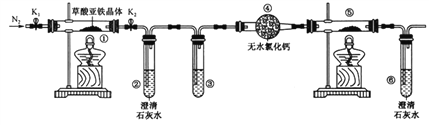
【题目】过氧化钠保存不当容易变质,某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取10.0g样品,并设计用如图装置来测定过氧化钠的质量分数。

上图中的E和F构成量气装置,用来测定O2的体积。
(1)写出以下装置发生反应的化学方程式:
装置A:___________________________。
装置B:___________________________。
装置C:____________________________。
(2)NaOH溶液的作用是_________________________。
(3)为准确读出氧气的体积需以下操作,正确的顺序为_________。
A.调整量筒高度,使广口瓶E与量筒F内液面相平
B.将气体冷却至室温
C.平视,使凹液面最低点与视线水平相切再读数
读出量筒内水的体积后,折算成标准状况氧气的体积为1.12L,则样品中过氧化钠的质量分数为_________。
【答案】CaCO3+2HCl=CaCl2+H2O+CO2↑NaHCO3+HCl=NaCl+H2O+CO2↑2Na2O2+2CO2=2NaCO3+O2(2Na2O2+2H2O=4NaOH+O2↑)吸收未反应的CO2 BAC78%
【解析】
根据实验原理可知A装置盐酸和大理石反应制取二氧化碳,B装置用来除去挥发的氯化氢,C装置中过氧化钠和二氧化碳反应,D装置用来吸收未反应的二氧化碳,E、F用来量取生成气体的体积,依据量筒读取液体体积时需要先冷却至室温及和集气瓶液面相平确定操作顺序;依据生成氧气的体积计算物质的量,结合化学方程式计算得到过氧化钠物质的量,从而得到过氧化钠的质量分数。
(1)装置A用来制备二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;装置B用来除去生成的二氧化碳中含有的氯化氢,和碳酸氢钠反应生成氯化钠、二氧化碳和水,反应的方程式为NaHCO3+HCl=NaCl+H2O+CO2↑;C装置中过氧化钠和二氧化碳以及水反应生成碳酸钠、氢氧化钠和氧气,反应方程式为2Na2O2+2CO2=2NaCO3+O2、2Na2O2+2H2O=4NaOH+O2↑;
(2)氢氧化钠和二氧化碳反应,吸收二氧化碳,便于测量氧气的体积,即氢氧化钠溶液的作用是吸收吸收未反应的CO2,便于测量氧气的体积;
(3)直接读取气体体积,不冷却到室温,会使溶液体积增大,读出结果产生误差,故应先冷却至室温,调整量筒内外液面高度使之相同,使装置内压强和外界压强相同,视线与凹液面的最低点相平读取量筒中水的体积是正确的读取方法,故操作顺序为BCA;
测定出量筒内水的体积后,折算成标准状况下氧气的体积为1.12L,物质的量为1.12L÷22.4L/mol=0.05mol,则样品中过氧化钠的物质的量是0.05mol×2=0.1mol,质量分数为![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】CoCl26H2O是一种饲料营养强化剂。可由水钴矿[主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等]制取,其工艺流程如下:
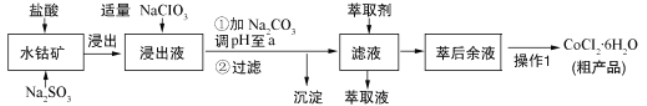
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等.
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl26H2O熔点为86℃,加热至110﹣120℃时,失去结晶水生成CoCl2.
回答下列问题:
(1)浸出水钴矿过程中,Fe2O3发生反应的化学方程式为________________________。
(2)向浸出液中加入适量NaClO3目的是______________________________________。
(3)“加Na2CO3调pH至a”,a=______;过滤所得沉淀的主要成分为_________(填化学式)。
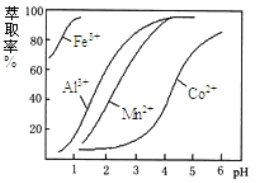
(4)萃取剂对金属离子的萃取与溶液pH的关系如下图所示,向“滤液”中加入该萃取剂的目的是__________,使用该萃取剂的最佳pH范围是_____(填选项字母)
A. 5.0﹣5.5 B. 4.0﹣4.5 C. 3.0﹣3.5 D. 2.0﹣2.5
(5)实验操作“操作1”为_______________、_________、过滤和减压烘干;制得的CoCl26H2O在烘干时需减压烘干的原因是________________________。