题目内容
【题目】下列有关实验的说法中,正确的是
A.容量瓶、滴定管、分液漏斗使用前都要检查是否漏液
B.配制1.00![]() 和4%的NaOH溶液,所用实验用品完全相同
和4%的NaOH溶液,所用实验用品完全相同
C.用稀硫酸溶液洗涤并灼烧铂丝后,再进行焰色反应
D.用广泛pH试纸测得0.10![]() NaHCO3溶液的
NaHCO3溶液的![]()
【答案】A
【解析】
A. 容量瓶、滴定管、分液漏斗等有活塞或瓶塞的仪器,使用前都要检查是否漏液,故A正确;
B. 配制1.00![]() 和4%的NaOH溶液,前者需要容量瓶,后者不需要容量瓶,故所用实验用品不完全相同,故B错误;
和4%的NaOH溶液,前者需要容量瓶,后者不需要容量瓶,故所用实验用品不完全相同,故B错误;
C. 用稀硫酸溶液洗涤并灼烧铂丝后,会生成沸点较高的硫酸盐附着在铂丝上,而用盐酸洗涤生成的氯化物的沸点较低,灼烧时容易除去杂质,故C错误
D. 用广泛pH试纸测试结果为大概的范围,精确度较差,比色卡显示的数值都为整数,故D错误;
答案选A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
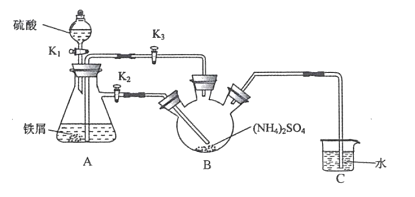
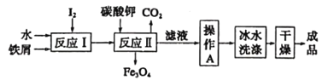
小学生10分钟应用题系列答案【题目】废旧电池的回收处理,既能减少对环境的污染,又能实现资源的再生利用。将废旧锌锰电池初步处理后,所得废料含MnO2、MnOOH、Zn(OH)2及少量Fe等,用该废料制备Zn和MnO2的一种工艺流程如下:
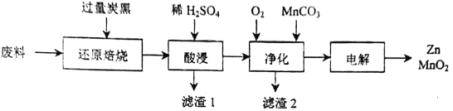
已知:
①Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化
②有关Ksp数据如下表所示
化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-13 | 10-17 | 10-38 |
回答下列问题:
(1)还原焙烧过程中, MnOOH与炭黑反应,锰元素被还原为MnO,该反应的化学方程式为___________。传统的工艺是使用浓盐酸在加热条件下直接处理废料,缺点是___________。
(2)酸漫时一般会适当加热并不断搅拌,其作用是___________,滤渣1和滤渣2主要成分的化学式依次是___________。
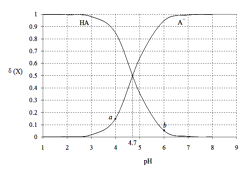
(3)净化时,先通入O2再加入MnCO3,其目的是___________;已知净化时溶液中Mn2+、Zn2+的浓度约为0.1mol·L-1,调节pH的合理范围是___________。
(4)电解制取MnO2时,MnO2在___________极产生。
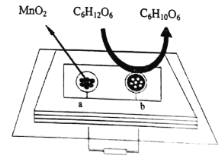
(5)中科院研究人员将MnO2和生物质置于一个由滤纸制成的折纸通道内形成电池,该电池可将软饮料中的葡萄糖作为燃料获得能量,装置如图所示。此装置中b极的电极反应式为______________________。