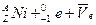题目内容
短周期元素A、B、C的核电荷数依次增多,它们原子的最外层电子数之和为10。A与C在同主族,B原子的最外层电子数等于A原子的次外层电子数,有关判断正确的是( )
A.原子半径A>B>C
B.气态氢化物稳定性A>B
C.A、B、C在同一周期
D.最高氧化物水化物酸性C>A
A.原子半径A>B>C
B.气态氢化物稳定性A>B
C.A、B、C在同一周期
D.最高氧化物水化物酸性C>A
B
由A、C为同主族元素可知它们的最外层电子数相同。因A、B、C按原子序数增加顺序排列,A应为第2周期元素,因第1周期元素无次外层电子,由此可知A的次外层具有2个电子(K层),据题意,B的最外层有2个电子。既然A、C的最外层电子数相同,由A、B、C最外层共10个电子,可得A、C最外层应各具4个电子。A、B、C分别是碳、镁、硅。其原子半径:Mg>Si>C,A不正确。气态氢化物稳定性CH4>SiH4,即B正确。最高价氧化物水化物的酸性应是非金属性相对强的强,即H2SO3>H2SiO3,D不正确。

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
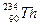 的原子来说( )
的原子来说( )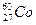 放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。
放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。