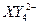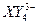题目内容
在下列粒子半径的比较中,正确的是( )
| A.Na+>Na | B.Cl->Cl |
| C.Ca2+>Cl- | D.Mg>Na |
B
阳离子的半径比其原子半径小,阴离子半径比其原子半径大,所以A错B对;Ca2+和Cl-均具有和Ar原子相同的电子层结构,因Ca2+的核电荷数大,故半径Ca2+<Cl-,C错误;Mg和Na的原子核外电子层数相同,Mg的核电荷数大于Na,则Mg的原子半径小于Na,D错误。

练习册系列答案
相关题目