题目内容
如图是短周期元素周期表的一部分,下列说法中正确的是( )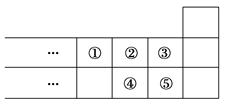
| A.元素①位于第二周期第ⅣA族 |
| B.气态氢化物的稳定性:④>② |
| C.最高价氧化物对应水化物的酸性:⑤>④ |
| D.元素的最高正化合价:③=⑤ |
C
解析

练习册系列答案
相关题目
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是( )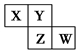
| A.元素W的最高价氧化物对应水化物的酸性最强 |
| B.单核阴离子半径的大小顺序为:r(W)>r(Z) >r(Y) |
| C.元素Y和元素Z的氢化物中均只存在极性共价键 |
| D.元素Y和元素Z的最高正化合价相同 |
W、X、Y、Z是短周期元素,其部分性质如下表
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的2/3 |
| Z | 第三周期原子半径最小的金属 |
下列说法正确的是
A.Z的氧化物属于碱性氧化物
B.最高价氧化物对应水化物的酸性:Y>X
C.离子半径:Z>W
D.气态氢化物的热稳定性:X>W
在元素周期表短周期元素中,X元素与Y、Z、W三元素相邻,X、Y的原子序数之和等于Z的原子序数,这四种元素原子的最外层电子数之和为20。下列判断正确的是
| A.四种元素的原子半径:rZ>rX>rY>rw |
| B.X、Y、Z、W形成的单质最多有6种 |
| C.四种元素均可与氢元素形成18电子分子 |
| D.四种元素中,Z的最高价氧化物对应水化物酸性最强 |
一种比黄金贵百倍的18O2气体,不久前在兰州近代物理研究所研究成功。1 mol这种18O2气体中含中子的物质的量为( )。
| A.10 mol | B.16 mol | C.20 mol | D.36 mol |
下列说法错误的是( )
| A.Na与Al为同周期元素,钠原子最外层有1个电子,铝原子最外层有3个电子,所以钠的金属性比铝强 |
| B.Na与Mg为同周期元素,且Mg的核电荷数比Na的大,所以钠的金属性比镁强 |
| C.NaOH为强碱,而Al(OH)3具有两性,所以钠的金属性比铝强 |
| D.Zn+2Fe3+=Zn2++2Fe2+,所以Zn的金属性比Fe强 |
2010年12月3日美国宇航局表示,在地球上发现全新的微生物,它能利用砷代替磷进行新陈代谢,砷含有剧毒。磷一直被认为是生命的6大基本元素,这种细菌的发现或说明可以扩大有机体生存条件及存在可能。下列关于砷和磷两种元素的叙述不正确的是( )
| A.它们的原子最外层电子数相等,元素的最高正化合价都是+5 |
| B.氮的非金属性比砷强,所以NH3的稳定性大于AsH3 |
| C.因为氮的原子半径比砷的小,所以氮的相对原子质量比砷的相对原子质量小 |
| D.它们都是主族元素 |
某短周期元素原子最外层只有2个电子,则该元素( )
| A.一定是第ⅡA族元素 |
| B.一定是金属元素 |
| C.一定是化合物中呈+2价元素 |
| D.可能是金属元素,也可能是非金属元素 |
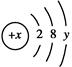 。
。