题目内容
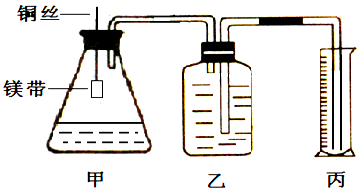
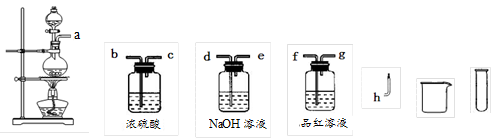
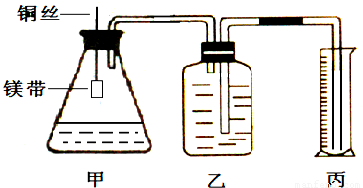
某小组为证明同温同压下,同浓度,同体积的酸性不同的两种二元酸与足量镁带反应时生成H2量相同而反应速率不同,装置如图.主要步骤如下:
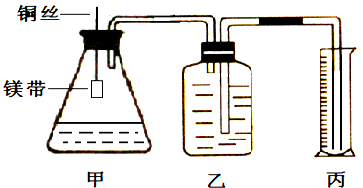
(1)配制浓度为0.5mol/L的硫酸和草酸溶液;
(2)用______量取10.00mL0.5mol/L的硫酸和草酸溶液分别加入两锥形瓶中;
(3)分别取去表面氧化膜的鎂带系于铜丝末端;
(4)检查装置气密性,乙中装满水,按图连接好装置;
(5)将铜丝下移,使足量鎂带浸如酸中(铜丝不与酸接触)至完全反应,同时记录______;
(6)反应结束时,读取量筒内水体积ymL.
将以上步骤补充完整并回答下列问题
(1)(4)中如何检查气密性______;
(2)用ρ=1.84 98.3%的浓硫酸配制250mL,c=0.5mol/L硫酸,主要仪器有______、______、烧杯、玻璃棒、酸式滴定管等;
(3)读取量筒内水体积时,必须注意的问题是______;
(4)简述速率不等的原因______,铜丝不能与酸接触的原因______;
(5)此实验说明草酸为弱酸,请再设计一实验证明:______.

(1)配制浓度为0.5mol/L的硫酸和草酸溶液;
(2)用______量取10.00mL0.5mol/L的硫酸和草酸溶液分别加入两锥形瓶中;
(3)分别取去表面氧化膜的鎂带系于铜丝末端;
(4)检查装置气密性,乙中装满水,按图连接好装置;
(5)将铜丝下移,使足量鎂带浸如酸中(铜丝不与酸接触)至完全反应,同时记录______;
(6)反应结束时,读取量筒内水体积ymL.
将以上步骤补充完整并回答下列问题
(1)(4)中如何检查气密性______;
(2)用ρ=1.84 98.3%的浓硫酸配制250mL,c=0.5mol/L硫酸,主要仪器有______、______、烧杯、玻璃棒、酸式滴定管等;
(3)读取量筒内水体积时,必须注意的问题是______;
(4)简述速率不等的原因______,铜丝不能与酸接触的原因______;
(5)此实验说明草酸为弱酸,请再设计一实验证明:______.
酸溶液应用酸式滴定管量取,如用碱式滴定管会腐蚀橡胶管;比较化学反应速率,必须是比较一定时间之内的反应物浓度的变化或其它量的变化,故答案为:酸式滴定管;反应所需时间;
(1)如不漏气,加热时容器内压强增大,会有气泡冒出,故答案为:往丙中加水没过导气管口下端,两手掌紧贴甲外壁一会儿,若观察到丙中导气管冒气泡,表明装置不漏气;
(2)配制溶液所需仪器有:250ml容量瓶、烧杯、玻璃棒、量筒或滴定管、胶头滴管等.故答案为:250ml容量瓶、胶头滴管;
(3)读数时要保持左右气体压强相等,以减少误差,故答案为:读数时保持乙丙中液面相平;待装置冷却至室温再读数;
(4)影响化学反应速率的因素有浓度、温度、压强等,本题为浓度不同,为测定镁与酸反应的速率,不能将铜丝与酸接触,否则易形成原电池,加快反应速率,干扰实验测定,
故答案为:H+浓度不同;与铜易形成原电池,加快反应速率,干扰实验测定;
(5)弱电解质存在电离平衡、不完全电离等性质,可任意选择合理方法,故答案为:测定草酸钠溶液的PH,如大于7,则为弱酸(其它合理答案也可以).
(1)如不漏气,加热时容器内压强增大,会有气泡冒出,故答案为:往丙中加水没过导气管口下端,两手掌紧贴甲外壁一会儿,若观察到丙中导气管冒气泡,表明装置不漏气;
(2)配制溶液所需仪器有:250ml容量瓶、烧杯、玻璃棒、量筒或滴定管、胶头滴管等.故答案为:250ml容量瓶、胶头滴管;
(3)读数时要保持左右气体压强相等,以减少误差,故答案为:读数时保持乙丙中液面相平;待装置冷却至室温再读数;
(4)影响化学反应速率的因素有浓度、温度、压强等,本题为浓度不同,为测定镁与酸反应的速率,不能将铜丝与酸接触,否则易形成原电池,加快反应速率,干扰实验测定,
故答案为:H+浓度不同;与铜易形成原电池,加快反应速率,干扰实验测定;
(5)弱电解质存在电离平衡、不完全电离等性质,可任意选择合理方法,故答案为:测定草酸钠溶液的PH,如大于7,则为弱酸(其它合理答案也可以).

练习册系列答案
相关题目