题目内容
【题目】黑灰的主要成分是硫化钡(BaS),常用于制取氧化钡等钡盐。
I.工业上常用如下方案测定黑灰中BaS含量:
步骤:准确称取一定质量黑灰试样置于烧杯中,加入适量的蒸馏水使黑灰充分溶解。
步骤2:过滤并洗涤残留固体2~3次,将滤液、洗涤液合并后完全转移至500mL容量瓶中,加水定容。
步骤3:取20.00mL步骤2中溶液于锥形瓶中,再迅速加入10mL2%醋酸稀溶液及25.00mL 0.5mo1/L碘标准溶液(过量),充分振荡,使BaS完全转化为S。
步骤4向锥形瓶中加入2-3滴淀粉溶液,用0.1mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液体积VmL(I2+2S2O32-=2I-+S4O62-)。
步骤5....
步骤6数据处理,计算黑灰中BaS含量。
(1)步骤2实验中所需的玻璃仪器有烧杯、漏斗.500mL容量瓶、_______。
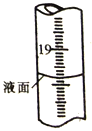
(2)步骤4到达滴定终点时,滴定管中液面如图所示,此时滴定管读数为____mL。若盛装Na2S2O3标准溶液的滴定管未润洗,则所测得的BaS含量将会_______(填“偏高”、“偏低"或“不变”)。
(3)为保证实验结果的准确性,步骤5应为_______________。
II.氯化钡可用于测定煤矿酸性矿井水中硫酸盐的含量。
(1)酸性矿井水(主要含有H+、Fe2+、SO42-)是煤层中夹杂的硫铁矿(FeS2)被空气中氧气氧化所致,该反应的离子方程式为_______________。
(2)查阅资料发现铁元素的存在对SO2含量(mg/L)的测定结果影响较大。请补充完整测定酸性矿井水中SO42-含量的实验步骤:量取一定体积的酸性矿井水,________,根据采集的数据计算废水中SO42-含量。
(实验中须使用的试剂有:稀氨水、30%双氧水、1mol/LBaCl2溶液)
【答案】 、胶头滴管 19.80 偏低 重复步骤3、步骤4操作2-3次(或进行空白实验) 2FeS2+7O2+2H2O=2Fe2++4SO42-+4H+( 加入过量30%双氧水充分反应后,再向其中滴加稀氨水至不再产生沉淀,过滤并洗涤沉淀2~3次,将滤液、洗涤液合并后,加入过量1mol/LBaCl2溶液,将所得沉淀过滤、洗涤、烘干,称取所得固体质量
【解析】I.(1)步骤2实验为溶解、洗涤和配制一定物质的量浓度的溶液,所需的玻璃仪器有烧杯、漏斗.500mL容量瓶、胶头滴管;(2)滴定管0刻度在上,此时滴定管读数为19.80mL。若盛装Na2S2O3标准溶液的滴定管未润洗,则标准液被稀释,滴定时消耗的标准液偏多,所测得的碘偏多,则测得的BaS含量将会偏低;(3)为保证实验结果的准确性,步骤5应为重复步骤3、步骤4操作2-3次(或进行空白实验);II. (1)煤层中夹杂的硫铁矿(FeS2)被空气中氧气氧化生成酸性矿井水(主要含有H+、Fe2+、SO42-),反应的离子方程式为2FeS2+7O2+2H2O=2Fe2++4SO42-+4H+;(2)查阅资料发现铁元素的存在对SO2含量(mg/L)的测定结果影响较大。请补充完整测定酸性矿井水中SO42-含量的实验步骤:量取一定体积的酸性矿井水,加入过量30%双氧水充分反应后,再向其中滴加稀氨水至不再产生沉淀,过滤并洗涤沉淀2~3次,将滤液、洗涤液合并后,加入过量1mol/LBaCl2溶液,将所得沉淀过滤、洗涤、烘干,称取所得固体质量,根据采集的数据计算废水中SO42-含量。