题目内容
【题目】按要求填空
(1)干冰是固态CO2的俗称,常用于人工降雨,44g干冰与A,B,C,D有如图所示的转化关系,请完成如图中的方框. 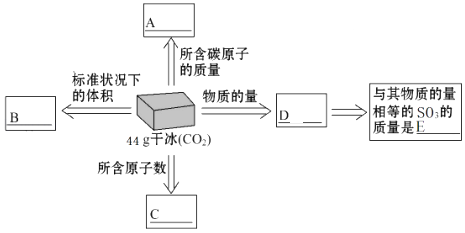
(2)标准状况下22.4L的HCl溶于水配成500mL溶液,所得溶液的物质的量浓度为 .
(3)配制1L 0.5molL﹣1NaOH溶液,需要1.25molL﹣1的NaOH溶液的体积是mL.
(4)19g MgX2含有Mg2+0.2mol,则MgX2的摩尔质量为 .
【答案】
(1)12g|22.4L|1.806×1024|1mol|64g
(2)2mol/L
(3)400
(4)95g/mol
【解析】解:(1)D.44g干冰的物质的量为: ![]() =1mol;
=1mol;
B.标准状况下该二氧化碳占有的体积为:1mol×22.4L/mol=22.4L;
C.所含原子物质的量为干冰的3倍,含有原子数目=1mol×3×6.02×1023mol﹣1=1.806×1024;
A.根据C原子守恒得n(C)=n(CO2),C原子的质量m=nM=1mol×12g/mol=12g;
E.三氧化硫与二氧化碳的物质的量相等,则该三氧化硫的质量m=nM=1mol×64g/mol=64g,
故答案为:12g;22.4L;1.806×1024;1mol;64g;(2)n(HC)= ![]() =1mol,c(HCl)=
=1mol,c(HCl)= ![]() =2mol/L,故答案为:2mol/L;(3)1L 0.5molL﹣1NaOH,配制过程中氢氧化钠的物质的量不变,则需要1.25molL﹣1的NaOH溶液的体积=
=2mol/L,故答案为:2mol/L;(3)1L 0.5molL﹣1NaOH,配制过程中氢氧化钠的物质的量不变,则需要1.25molL﹣1的NaOH溶液的体积= ![]() =0.4L=400mL,故答案为:400;(4)19g MgX2含有Mg2+0.2mol,根据Mg原子守恒得,n(MgX2)=n(Mg )=0.2mol,则MgX2的摩尔质量为:M(MgX2)=
=0.4L=400mL,故答案为:400;(4)19g MgX2含有Mg2+0.2mol,根据Mg原子守恒得,n(MgX2)=n(Mg )=0.2mol,则MgX2的摩尔质量为:M(MgX2)= ![]() =95g/mol,故答案为:95g/mol.
=95g/mol,故答案为:95g/mol.
(1)根据n= ![]() 计算44g干冰的物质的量,根据V=nVm计算标况下占有的体积,所含原子物质的量为干冰的3倍,再根据N=nNA计算含有原子数目,碳原子物质的量等于干冰的物质的量,根据m=nM计算含有碳原子的质量;三氧化硫与二婚头物质的量相等,根据m=nM计算三氧化硫的质量;(2)根据n=
计算44g干冰的物质的量,根据V=nVm计算标况下占有的体积,所含原子物质的量为干冰的3倍,再根据N=nNA计算含有原子数目,碳原子物质的量等于干冰的物质的量,根据m=nM计算含有碳原子的质量;三氧化硫与二婚头物质的量相等,根据m=nM计算三氧化硫的质量;(2)根据n= ![]() 计算HCl的物质的量,再根据c=
计算HCl的物质的量,再根据c= ![]() 计算所得溶液物质的量浓度;(3)根据稀释定律计算需要1.25molL﹣1的NaOH溶液的体积;(4)根据M=
计算所得溶液物质的量浓度;(3)根据稀释定律计算需要1.25molL﹣1的NaOH溶液的体积;(4)根据M= ![]() 计算MgX2的摩尔质量.
计算MgX2的摩尔质量.