题目内容
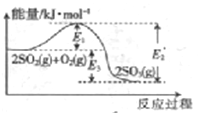
【题目】工业制硫酸的主要反应之一为2SO2(g)+O2(g)![]() 2SO3(g),反应过程中能量变化如图所示,下列说法错误的是
2SO3(g),反应过程中能量变化如图所示,下列说法错误的是
A. 该反应的正反应为放热反应 B. 向反应体系中加入催化剂后,图中E3不变
C. 该反应的焓变△H=(E1-E2)kJ/mol D. 升高温度,E1变大
【答案】D
【解析】图中E1为正反应的活化能,E2为逆反应的活化能,E3为反应热。A项,由于反应物的总能量大于生成物的总能量,该反应的正反应为放热反应,正确;B项,催化剂能改变反应的历程,降低反应的活化能,不改变反应热,加入催化剂后E1、E2减小,E3不变,正确;C项,该反应的焓变ΔH=(E1-E2)kJ/mol,正确;D项,升高温度,使分子获得更高的能量,增大活化分子百分数,E1不变,错误;答案选D。

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目