题目内容
【题目】A、B都是芳香族化合物,![]() 水解得到
水解得到![]() 和1mol醋酸。A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O。且B分子中碳和氢元素总的质量分数为65.2%。A溶液具有酸性,不能使氯化铁溶液显色。
和1mol醋酸。A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O。且B分子中碳和氢元素总的质量分数为65.2%。A溶液具有酸性,不能使氯化铁溶液显色。
(1)A、B相对分子质量之差为____________________。
(2)1个B中应该有____________________个氧原子。
(3)A的分子式为____________________。
【答案】42 3 ![]()
【解析】
A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O.且B分子碳和氢元素总的质量百分含量为65.2%,根据B+CH3COOH→A+H2O判断,假设A的相对分子质量为200,则B的最大相对分子质量为156,含氧34.8%,则氧原子个数为![]() ≈3,即B分子中含有3个O原子,则有机物B的相对分子质量=
≈3,即B分子中含有3个O原子,则有机物B的相对分子质量=![]() =138,A溶液具有酸性,1molA水解得到1molB和1mol醋酸,可知B中含有-COOH、-OH,B分子是去掉1个-COOH、-OH属于基团的式量=138-45-17=76,则属于基团中C原子最大数目为
=138,A溶液具有酸性,1molA水解得到1molB和1mol醋酸,可知B中含有-COOH、-OH,B分子是去掉1个-COOH、-OH属于基团的式量=138-45-17=76,则属于基团中C原子最大数目为![]() =6…4,故为-C6H4-,B的分子式为C7H6O3;根据B+CH3COOH→A+H2O可知A的分子式为C9H8O4。
=6…4,故为-C6H4-,B的分子式为C7H6O3;根据B+CH3COOH→A+H2O可知A的分子式为C9H8O4。
(1)根据B+CH3COOH→A+H2O可知,Mr(A)-Mr(B)=Mr(CH3COOH)-Mr(H2O)=60-18=42;
(2)根据以上分析可知B中含有3个氧原子;
(3)根据分析可知A的分子式为C9H8O4。

【题目】以方铅矿(PbS)为原料制备铅蓄电池的电极材料的工艺流程如图所示: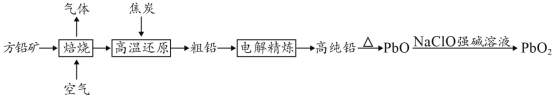
请回答下列问题:
(1)“焙烧”生成的气体直接排放可能造成的环境问题是____________,“焙烧”前须将方铅矿研磨粉粹的目的是________________________________。
(2)电解时,如c(Pb2+)远大于c(H+),则Pb2+优先于H+放电,工业上应用此原理可对铅进行电解精炼。“粗铅”的杂质主要有锌、铁、铜、银等,则阳极泥的主要成分为_________。
(3)写出制备PbO2的离子方程式________________________。
(4)已知部分含铅化合物的Ksp如下表所示:
物质 | PbCl2 | PbS |
Ksp | 1.2×10-5 | 9.0×10-29 |
①铅与稀盐酸反应产生少量气泡后反应终止,原因是_____________________。
②Pb(NO3)2是强酸弱碱盐,氢硫酸是弱酸[Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.1×10-15],已知K>105时可以认为反应基本完全,通过计算判断向Pb(NO3)2溶液中通入H2S气体能否形成PbS沉淀___________________。(要求写出计算过程)