题目内容
关于如图所示①、②两个装置的评价正确的是
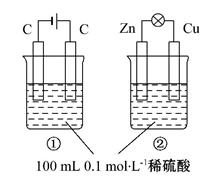

| 选择 | 叙 述 | 评价 |
| A | 装置名称:①电解池,②原电池 | 错误 |
| B | 硫酸浓度变化:①增大,②减小 | 错误 |
| C | 电极反应式:①阳极:4OH--4e-====2H2O+O2↑ ②正极:Zn-2e-====Zn2+ | 正确 |
| D | 离子移动方向:①H+向阴极移动 ②H+向正极移动 | 正确 |
D
试题分析:A、装置①外加了电源,为电解池,装置②形成Zn、Cu原电池,叙述正确;B、电解稀硫酸实质是电解水,所以装置①中硫酸浓度增大,装置②的总反应为:Zn+H2SO4=ZnSO4+H2↑,硫酸浓度减小,叙述正确;C、电解硫酸溶液的阳极为OH?失电子:4OH--4e-=2H2O+O2↑,原电池的正极为H+得电子:2H++2e?=H2↑,叙述错误;D、电解池电解质溶液中阳离子向阴极移动,原电池电解质溶液中阳离子向正极移动,正确。

练习册系列答案
相关题目
 C+LiCoO2锂硫电池的总反应为:2Li+S
C+LiCoO2锂硫电池的总反应为:2Li+S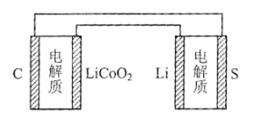
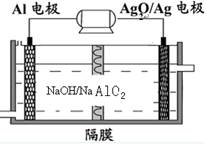

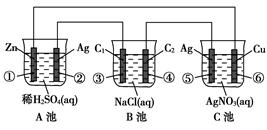
 2CO2+4H2O
2CO2+4H2O