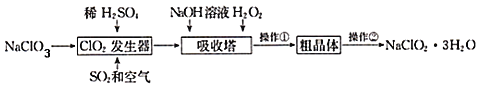
��Ŀ����
����Ŀ���о�������Ⱦ��Ĵ������Ի��������������Ⱦ������������������ĵ�����ʮ����Ҫ�����塣
(1)��֪��C(s)+O2(g)�TCO2(g)��H����393.5/kJmol
N2(g)+O2(g)�T2NO(g)��H��+180kJ/mol
��C(s)+2NO(g)�TCO2(g)+N2(g) ����H��_____kJ/mol��
(2)��һ���¶��£���2L�ĺ����ܱ������г���4.0 mol NO2��4.0 mol CO���ڴ��������·�����Ӧ4CO(g)+2NO2(g)4CO2(g)+N2(g)�����������������ʾ��
t/min | 0 | 5 | 10 | 15 | 20 |
n(NO2)/mol | 4.0 | 3.4 | 3.12 | 3.0 | 3.0 |
n(N2)/mol | 0 | 0.30 | 0.44 | 0.50 | 0.50 |
����0��5 min�ڣ���CO2��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ_____��
�ڴ��¶��µĻ�ѧƽ�ⳣ��K�ı���ʽΪ_____��
(3)�û���̿��ԭ��������������йط�ӦΪC(s)+2NO(g)![]() CO2(g)+N2(g)��ij�о�С����2L�ܱ������м��������Ļ���̿��һ������NO�������¶Ⱥ�������䣬����������Ӧ��
CO2(g)+N2(g)��ij�о�С����2L�ܱ������м��������Ļ���̿��һ������NO�������¶Ⱥ�������䣬����������Ӧ��
������������˵��������Ӧ�Ѵ�ƽ�����_____(����)��
A.����̿���������ٱ仯
B.������������ܶȱ��ֲ���
C.2v(NO)�� ��v(N2)��
D.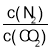 ���ֲ���
���ֲ���
��ѹǿΪpʱ�������Ĵ�Ч�ʡ������������������¶ȵĹ�ϵ��ͼ��ʾ��������������������Ҫȡ�����¶�ʱ����Ӧ���¶ȷ�Χ��_____��

(4)��(N2H4)����ɫҺ�壬����ǿ��ԭ�ԡ�
���µ�ˮ��Һ�������ԣ�����������NH3H2O���ƣ����һ�����뷽��ʽΪ_____��
������N2H4ȼ�ϵ�ز���Ի���û����Ⱦ���õ���Թ���������Ϊ�����(�ܴ���O2��)��д�������ĵ缫��Ӧʽ_____��
���𰸡���573.5 0.012mol/��Lmin�� K��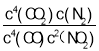 AB 300��400�� N2H4H2ON2H5++OH�� N2H4��4e��+2O2����N2��+2H2O
AB 300��400�� N2H4H2ON2H5++OH�� N2H4��4e��+2O2����N2��+2H2O
��������
(1)����֪��C(s)+O2(g)�TCO2(g)��H����393.5kJ/mol
N2(g)+O2(g)�T2NO(g)��H��+180kJ/mol
�ɸ�˹���ɼ���٩��ڵõ�C(s)+2NO(g)�TCO2(g)+N2(g) ��
(2) �١�����v=![]() ���㣻
���㣻
�ڡ�����ƽ�ⳣ������ʽ���
(3) �١����ݷ�Ӧ���淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ�������(ͬ������)�����淴Ӧ����֮�ȵ���ϵ��֮��(��ͬ����)��ƽ��ʱ�������ʵ����ʵ�����Ũ�ȵȲ��ٷ����仯���ɴ�������һЩ���������䣬�Դ˷�����
�ڡ�����������������Ҫȡ�����¶�ʱ��˵����ʱҪ�Ѵ������Խ�����ͻ��ߴ�Ч�ʻ������ֲ���ʱ�����������¶�������N2�����������ӣ���
(4) �١��µ�ˮ��Һ�������ԣ�����������NH3H2O���ƣ����һ�����뷽��ʽΪ��N2H4H2ON2H5++OH������N2H4+H2ON2H5++OH������
�ڡ�ȼ�ϵ�ظ�������������Ӧ��N2H4ת��ΪN2���ݴ˽��
��1����֪����C��s��+O2��g���TCO2��g����H1����393.5/kJmol
��N2��g��+O2��g���T2NO��g����H2��+180kJ/mol
����ӦΪ��C��s��+2NO��g���TCO2��g��+N2��g������Ӧ���ɢ٩��ڵõ������ݸ�˹���ɣ���H����H1����H2����573.5kJ/mol��
�ʴ�Ϊ����573.5��
��2����0��5min�ڣ���n��N2����0.30mol����v��N2����![]() ��
��![]() ��0.003mol/��Lmin�����ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���v��CO2����4v��N2����0.012mol/��Lmin����
��0.003mol/��Lmin�����ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���v��CO2����4v��N2����0.012mol/��Lmin����
�ʴ�Ϊ��0.012mol/��Lmin����
�ڷ�ӦΪ��4CO��g��+2NO2��g��4CO2��g��+N2��g��������¶��µĻ�ѧƽ�ⳣ��K�ı���ʽΪK��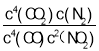 ���ʴ�Ϊ��K��
���ʴ�Ϊ��K��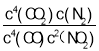 ��
��
��3����A������̿�μӻ�ѧ��Ӧ�����ŷ�Ӧ���У����������仯���ﵽ��ѧƽ��ʱ������̿�������䣬��Aѡ��
B��������������ܶ�Ϊ![]() ����Ӧǰ�������غ㣬�������й������ʲ��룬���������ᷢ���ı䣬����V���䣬�������̻�������ܶȸı䣬����ͨ���ܶȱ仯�жϻ�ѧƽ�⣬��Bѡ��
����Ӧǰ�������غ㣬�������й������ʲ��룬���������ᷢ���ı䣬����V���䣬�������̻�������ܶȸı䣬����ͨ���ܶȱ仯�жϻ�ѧƽ�⣬��Bѡ��
C����Ӧ�ﵽƽ��ʱ��v����v����ӦΪv ��NO������2v ��N2��������C��ѡ��
D��N2��CO2ʼ�հ�1��1�������ɣ����жϻ�ѧƽ�⣬��D��ѡ��
�ʴ�Ϊ��A��B��
�ڵ���������������Ҫȡ�����¶�ʱ��˵����ʱҪ�Ѵ������Խ�����ͣ����������¶�������N2�����������ӣ����Կ��Կ����¶ȵķ�Χ�ǣ�300��400�棬
�ʴ�Ϊ��300��400�棻
��4�����µ�ˮ��Һ�������ԣ�����������NH3H2O���ƣ����һ�����뷽��ʽΪ��N2H4H2ON2H5++OH������N2H4+H2ON2H5++OH������
�ʴ�Ϊ��N2H4H2ON2H5++OH������N2H4+H2ON2H5++OH������
��ȼ�ϵ�ظ�������������Ӧ��N2H4ת��ΪN2�����Ե缫��ӦΪ��N2H4��4e��+2O2����N2��+2H2O��
�ʴ�Ϊ��N2H4��4e��+2O2����N2��+2H2O��