题目内容
盖斯定律在生产和科学研究中有很重要的作用,有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。已知7.2 g碳在12.8g的氧气中燃烧,至反应物耗尽,放出x kJ热量。已知单质碳的燃烧热为y 
 则1 mol C与
则1 mol C与 反应生成CO的反应热
反应生成CO的反应热 H为
H为

 则1 mol C与
则1 mol C与 反应生成CO的反应热
反应生成CO的反应热 H为
H为A.-(2.5x -0.5 y)  | B.-(5x - 0.5y)   |
C.-(10x - y)  | D.- y  |
A
(1)C(s)+O2(g)=CO2(g);△H=-y
 (2)C(s)+1/2O2(g)=CO(g);△H=-z
(2)C(s)+1/2O2(g)=CO(g);△H=-z
 ,设发生(1)的碳为amol, 发生(2)的碳为bmol,则有12(a+b)=7.2,32(a+0.5b)="12.8" ,解得a=0.2 b=0.4 ay+bz=x,解得z=" -(2.5x" -0.5 y)
,设发生(1)的碳为amol, 发生(2)的碳为bmol,则有12(a+b)=7.2,32(a+0.5b)="12.8" ,解得a=0.2 b=0.4 ay+bz=x,解得z=" -(2.5x" -0.5 y) 


 (2)C(s)+1/2O2(g)=CO(g);△H=-z
(2)C(s)+1/2O2(g)=CO(g);△H=-z
 ,设发生(1)的碳为amol, 发生(2)的碳为bmol,则有12(a+b)=7.2,32(a+0.5b)="12.8" ,解得a=0.2 b=0.4 ay+bz=x,解得z=" -(2.5x" -0.5 y)
,设发生(1)的碳为amol, 发生(2)的碳为bmol,则有12(a+b)=7.2,32(a+0.5b)="12.8" ,解得a=0.2 b=0.4 ay+bz=x,解得z=" -(2.5x" -0.5 y) 


练习册系列答案
相关题目
 Si(s)+4HCl(g),计算该反应的反应热△H为 。
Si(s)+4HCl(g),计算该反应的反应热△H为 。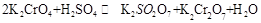
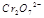 在水溶液中为红色,
在水溶液中为红色,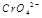 在水溶液中为黄色。某条件下该反应建立平衡后,体系为两种离子的混合液,颜色为橙色。
在水溶液中为黄色。某条件下该反应建立平衡后,体系为两种离子的混合液,颜色为橙色。 ;
;
 ,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用
,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用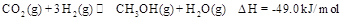
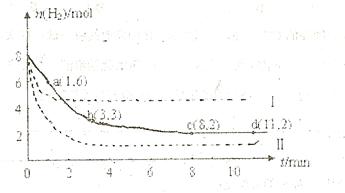
 充入一容积为2L的密闭容器中,测得H
充入一容积为2L的密闭容器中,测得H