题目内容
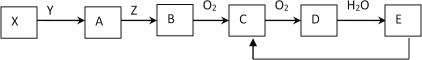
【题目】“长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分)。某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )

A. A为正极
B. 电池工作时H+由A极向B极迁移
C. 从b 口通入四氧化二氮气体且在B极发生氧化反应
D. A极发生的电极反应式:C2H8N2+4H2O+16e-=2CO2+N2+16H+
【答案】B
【解析】根据图中信息可知,外电路中电子从A电极流向B电极,所以A为负极,B为正极。内电路一般是阳离子各正极移动、阴离子向负极移动,所以电池工作时H+由A极向B极迁移。根据原电池原理,还原剂在负极上失去电子发生氧化反应,氧化剂在正极上得到电子发生还原反应,所以从a口通入的偏二甲肼发生氧化反应,从b口通入的四氧化二氮发生还原反应。由于产物都是空气中的成分,所以原电池反应的产物为二氧化碳、氮气和水。综上所述,B选项正确。

练习册系列答案
相关题目