题目内容
【题目】如图所示的过程是目前直接利用太阳能的研究热点。人们把通过人工光化学手段合成燃料的过程叫做人工光合作用。

(1)在上图构想的物质和能量循环中太阳能最终转化为__________能。
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)![]() 2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
①平衡时,氧气的物质的量浓度为____;用H2O(g)表示0~3 min内该反应的平均反应速率为_____。
②能说明该反应已达到平衡状态的是_____________。
A.n(CH3OH) :n(O2)=2 :3 B.容器内气体密度保持不变
C.容器内气体压强保持不变 D.υ正(H2O)=2υ逆(CO2)
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则氧气应通入该燃料电池的________极(填“正”或“负”),通入甲醇的一极的电极反应式为________________。
【答案】热 0.075 mol·L-1 0.03mol·L-1·min-1 CD 正 CH3OH - 6e- + H2O = CO2↑+6H+
【解析】
(1)图中太阳能最终以燃烧热的形式放出,即最终转化为热能。故答案:热;
(2)①将CO2和H2O转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)![]() 2CH3OH(g)+3O2(g),有表格数据可知4min时化学反应达到平衡。平衡时甲醇的物质的量为0.1mol, O2的物质的量为0.15mol,所以平衡时,氧气的物质的量浓度为c=0.15mol/2L=0.075 molL-1;0~3 min 内甲醇的物质的量变化0.09mol,根据2CO2(g)+4H2O(g)
2CH3OH(g)+3O2(g),有表格数据可知4min时化学反应达到平衡。平衡时甲醇的物质的量为0.1mol, O2的物质的量为0.15mol,所以平衡时,氧气的物质的量浓度为c=0.15mol/2L=0.075 molL-1;0~3 min 内甲醇的物质的量变化0.09mol,根据2CO2(g)+4H2O(g)![]() 2CH3OH(g)+3O2(g)可知,水变化的物质的量为0.18mol, 0~3 min内水的平均反应速率为v=0.18mol /(2L×3min)=0.03molL-1min-1 ;因此,本题正确答案是: 0.075 mol·L-1;0.03mol·L-1·min-1;
2CH3OH(g)+3O2(g)可知,水变化的物质的量为0.18mol, 0~3 min内水的平均反应速率为v=0.18mol /(2L×3min)=0.03molL-1min-1 ;因此,本题正确答案是: 0.075 mol·L-1;0.03mol·L-1·min-1;
②A.无论是否达到平衡状态,生成物的物质的量之比都等于化学计量数之比,即n(CH3OH) :n(O2)=2 :3 ,故A错误;
B.因气体的体积以及质量不变,则容器内密度保持不变,不能用于判断是否达到平衡状态,故B错误;
C.反应前后气体的体积不等,容器内压强保持不变,可说明达到平衡状态,故C正确;
D.v正(H2O)=2v逆(CO2),可说明正逆反应速率相等,达到平衡状态,故D正确;
因此,本题正确答案是:CD;
(3)甲醇、氧气和稀硫酸制作燃料电池中,氧气被还原生成水,做电池的正极,甲醇被氧化,做电池的负极 ,其电极方程式为CH3OH - 6e- + H2O = CO2↑+6H+,
因此,本题正确答案是:正; CH3OH - 6e- + H2O = CO2↑+6H+;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】高铁酸钾(K2FeO4)是一新型、高效、无毒的多功能水处理剂。
(资料)K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4。
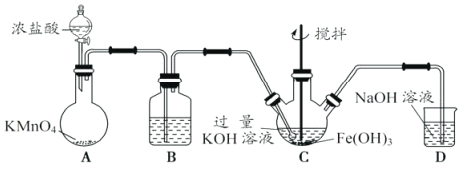
①A为制取氯气发生装置,其中盛放浓盐酸的仪器名称为___________。
②除杂装置B中的试剂为___________。
③C为制备K2FeO4装置,KOH溶液过量的原因是___________。
④D为尾气处理装置,发生反应的离子方程式为___________。
(2)探究 K2FeO4的性质。取C中紫色溶液,加入稀硫酸,产生黃绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计以下方案:
方案I | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
①由方案I中溶液变红可知a中含有___________。该离子的产生___________(填“能”或“不能”)判断一定是由K2FeO4被Cl-还原而形成的。
②方案Ⅱ用KOH溶液洗涤的目的是___________。方案Ⅱ得出氧化性:Cl2___________FeO42-(填“>”或“<”)
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:_______ FeO42-+______H+===_______O2↑+________Fe3++________(配平及完成上述离子方程式)________。现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为___________。(计算结果保留到0.1%)