题目内容
16.根据硝酸和硫酸所具有的性质,选择适当的字母按要求填空.A.吸水性B.脱水性C.强氧化性D.强氧化性和酸性
(1)浓硫酸常用作干燥剂,说明浓硫酸具有A;
(2)用玻璃棒蘸浓硫酸滴在纸上,发现变黑,说明浓硫酸具有B;
(3)浓硫酸和浓硝酸都可以与铜反应,反应中浓硫酸和浓硝酸显示出D.
分析 浓硫酸具有脱水性,可使蔗糖碳化,具有吸水性,可用作干燥剂,具有强氧化性,可与铜反应生成硫酸铜和二氧化硫,同时表现为酸性,以此解答.
解答 解:(1)浓硫酸具有吸水性,可用于干燥气体,故答案为:A;
(2)浓硫酸具有脱水性,用玻璃棒蘸浓硫酸滴在纸上,纤维素脱水而碳化,故答案为:B;
(3)浓硫酸、浓硝酸具有强氧化性,浓硫酸可与铜反应生成硫酸铜和二氧化硫,浓硝酸与Cu反应生成硝酸铜、二氧化氮,同时生成盐表现为酸性,故答案为:D.
点评 本题考查浓硫酸的性质,为高频考点,侧重于学生的分析能力和基础知识的综合运用的考查,注意把握浓硫酸的特性,题目难度不大.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
6.下列实验操作可以达到实验目的是( )
| A. | 用铝片与氧化铁混合加热进行铝热反应 | |
| B. | 将蔗糖溶于水,加热几分钟后再加人少量新制的Cu(OH)2就可实现将蔗糖水解,并用新制的Cu(OH)2检验蔗糖的水解产物 | |
| C. | 用溴的四氯化碳溶液就能鉴别乙烷与乙烯 | |
| D. | 向裂化汽油中加人酸性高锰酸钾溶液,振荡,紫色褪去说明汽油中含有甲苯等苯的同系物 |
7.下列有关物质性质的应用正确的是( )
| A. | 生石灰能与水反应,可用来干燥氯气 | |
| B. | 氯化铝是一种电解质,可用于电解法制铝 | |
| C. | 液氨汽化时要吸收大量的热,可用做制冷剂 | |
| D. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 |
4.化学与生产、生活密切相关.下列叙述正确的是( )
| A. | 使用含有氯化钠的融雪剂会加快桥梁的腐蚀 | |
| B. | “海水淡化”可以解决“淡水供应危机”,向海水中加入净水机明矾可以使海水淡化 | |
| C. | 煤经过气化、液化等物理变化可得到清洁燃料 | |
| D. | 棉花、羊毛、木材和草类的主要成分都是纤维素 |
11.下列离子方程式的书写正确的是( )
| A. | 在硫酸铜溶液中加入过量氢氧化钡溶液 Ba2++SO42-=BaSO4↓ | |
| B. | 钠与水的反应Na+2H2O═Na++2OH-+H2↑ | |
| C. | 氯气通入氢氧化钠溶液中 2Cl2+2OH-=3Cl-+ClO-+H2O | |
| D. | 大理石溶于醋酸的反应CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O |
1.已知常温下,0.1mol•L-1CH3COONH4溶液呈中性.下列有关叙述正确的是( )
| A. | 该溶液可由等体积、浓度均为0.1mol•L-1的醋酸和氨水反应得到 | |
| B. | CH3COONH4加人纯水中,水的电离程度不变 | |
| C. | 常温下,电离平衡常数K(CH3 COOH)=K(NH3•H2 O) | |
| D. | 该溶液中c(CH3 COO-)大于同浓度CH3 COONa溶液中的c(CH3 COO-) |
5. (1)利用Na2SO3溶液可脱除烟气中的SO2.Na2SO3可由NaOH溶液吸收SO2制得.NaOH溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如表:
(1)利用Na2SO3溶液可脱除烟气中的SO2.Na2SO3可由NaOH溶液吸收SO2制得.NaOH溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如表:
①由表判断,NaHSO3溶液显酸性,用化学平衡原理解释:溶液中存在:HSO3?SO32-+H+;HSO3-+H2O?H2SO3+OH-电离程度大于水解程度,故溶液显酸性.
②请写出Na2SO3溶液中离子浓度大小关系:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
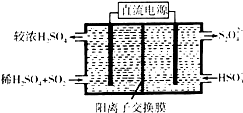
(2)利用图示装置(电极均为惰性电极)吸收SO2,由阴极排出的溶液可吸收NO2.
①阴极的电极反应式为2HSO3-+2H++2e-=S2O42-+2H2O.
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成.写出该反应离子方程式:4S2O42-+2NO2+8OH-═8SO42-+N2+4H2O.
(3)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收的产物反应,得到一种复合肥.
①该复合肥料可能的化学式为(NH4)3PO4(或(NH4)2HPO4或NH4H2PO4)(只写一种).
②若氨水与SO2恰好完全反应生成正盐,则此时溶液呈碱性(填“酸”“碱”或“中”).已知常温下NH3•H2O的Kb=1.8×10-5mol•L-1,H2SO3的Ka1=1.3×10-2mol•L-1Ka2=6.3×10-8mol•L-1.
③当氨水吸收SO2至恰好完全反应形成正盐时,反应过程中H2O的电离平衡移动方向为向右(填“向左”“向右”或“不”).
 (1)利用Na2SO3溶液可脱除烟气中的SO2.Na2SO3可由NaOH溶液吸收SO2制得.NaOH溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如表:
(1)利用Na2SO3溶液可脱除烟气中的SO2.Na2SO3可由NaOH溶液吸收SO2制得.NaOH溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如表:| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
②请写出Na2SO3溶液中离子浓度大小关系:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
(2)利用图示装置(电极均为惰性电极)吸收SO2,由阴极排出的溶液可吸收NO2.
①阴极的电极反应式为2HSO3-+2H++2e-=S2O42-+2H2O.
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成.写出该反应离子方程式:4S2O42-+2NO2+8OH-═8SO42-+N2+4H2O.
(3)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收的产物反应,得到一种复合肥.
①该复合肥料可能的化学式为(NH4)3PO4(或(NH4)2HPO4或NH4H2PO4)(只写一种).
②若氨水与SO2恰好完全反应生成正盐,则此时溶液呈碱性(填“酸”“碱”或“中”).已知常温下NH3•H2O的Kb=1.8×10-5mol•L-1,H2SO3的Ka1=1.3×10-2mol•L-1Ka2=6.3×10-8mol•L-1.
③当氨水吸收SO2至恰好完全反应形成正盐时,反应过程中H2O的电离平衡移动方向为向右(填“向左”“向右”或“不”).
6.不能作为判断硫、氯两种元素非金属性强弱的依据是( )
| A. | 单质氧化性的强弱 | |
| B. | 单质沸点的高低 | |
| C. | 单质与氢气化合的难易 | |
| D. | 最高价氧化物对应的水化物酸性的强弱 |
 研究金属铁及其化合物的性质有重要意义.
研究金属铁及其化合物的性质有重要意义.