��Ŀ����
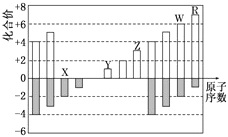
����Ŀ��Ԫ�������ڱ��е�λ�ã���ӳ��Ԫ�ص�ԭ�ӽṹ��Ԫ�ص����ʣ���ͼ��Ԫ�����ڱ���һ���֣�
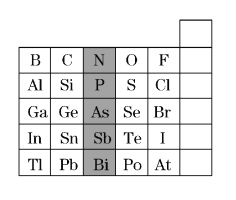
��1������Ԫ�������ɣ�����Ԥ�⣬H3AsO4��H3PO4������ǿ����H3AsO4________H3PO4(������������������������)��
��2������NaH�Ĵ��ڣ���������ɰ���Ԫ�ط��ڵ���A�壬��ô�������������������۵ľ���ֵ��ȣ��ֿɰ���Ԫ�ط������ڱ��еĵ�________�壮
��3��Ԫ�ؼ��ǵ������ڽ���Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ���Ԫ�ص������������ˮ��Ӧ�����ӷ���ʽΪ��__________________________________________________________.
��4�����ڱ�����10���������������Ԫ�أ�������һ�ֱ���Ϊ������Ԫ����������Ԫ��R�����ӳ���������������Ҫ���ã���֪RԪ�ص�ԭ����4�����Ӳ㣬�����������ķ���ʽΪRO3����RԪ�ص�����Ϊ : _____________________________________.
��5���ʻ���(COS)���ӽṹ�������̼���ӽṹ���ƣ�����ԭ�ӵ�����㶼����8���ӽṹ���õ���ʽ��ʾ�ʻ�����ӵ��γɹ��̣�_____________________________________.
���𰸡� �� ��A Al3����3NH3��H2O===Al(OH)3����3NH![]() ��
�� ![]()
��������(1)NԪ��ԭ����2�����Ӳ�������������Ϊ5��λ��Ԫ�����ڱ��еڶ����ڵ���A����ͬ������ϵ��·ǽ����Լ���������ۺ����������Խ����������![]() ����ȷ��: �� ��
����ȷ��: �� ��
(2)�����������������۵ľ���ֵ���������Ԫ�ط������ڱ��е���A������ȷ��:��A��
(3)Ԫ�ؼ��ǵ������ڽ���Ԫ����ԭ�Ӱ뾶��С��Ԫ�������ΪAl���������������ˮ��Ӧ������������������笠���������Ӧ���ӷ���ʽΪ: Al3����3NH3��H2O===Al(OH)3����3NH![]() ����ȷ��: Al3����3NH3��H2O===Al(OH)3����3NH
����ȷ��: Al3����3NH3��H2O===Al(OH)3����3NH![]() ��
��
(4)RԪ�ص�ԭ����4�����Ӳ��������������ķ���ʽΪ![]() ������������Ϊ6�����ڵ���������A����ΪSeԪ������ȷ��������
������������Ϊ6�����ڵ���������A����ΪSeԪ������ȷ��������
(5)�ʻ���![]() ���ӽṹ�������̼���ӽṹ����������ԭ�ӵ�����㶼����8���ӽṹ����C��O��C��S���γ����Թ��е��Ӷ��� COS�ĵ���ʽΪ
���ӽṹ�������̼���ӽṹ����������ԭ�ӵ�����㶼����8���ӽṹ����C��O��C��S���γ����Թ��е��Ӷ��� COS�ĵ���ʽΪ![]() ���õ���ʽ��ʾ�ʻ�����ӵ��γɹ���Ϊ
���õ���ʽ��ʾ�ʻ�����ӵ��γɹ���Ϊ![]() ����ȷ����
����ȷ����![]() ��
��

����Ŀ���������ɴ�������β����2NO+2CO2CO2+N2 �� ij�¶������ݻ�������ܱ�������ͨ��NO ��CO����ͬʱ��NO ��CO ��Ũ�����±�������˵���в���ȷ���ǣ� ��
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
c��NO��/��10��3molL��1 | 1.00 | 0.45 | 0.25 | 0.15 | 0.10 | 0.10 |
c��CO��/��10��3molL��1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
A.2 s �ڵ�ƽ����Ӧ���ʦԣ�N2��=1.875��10��4 molL��1s��1
B.�ڸ��¶���K=5
C.�����ݻ���СΪԭ����һ�룬NO ת���ʴ���90%
D.ijʱ���ٳ���0.1 mol NO��0.36 mol CO�����´�ƽ���CO Ũ�ȱ�ԭƽ���