��Ŀ����
����Ŀ��̼��������ֽ����������֯���Ƹ����ҵ����Ҫԭ�ϡ���ҵ̼����(����ԼΪ98%)�к���Mg2+��Fe3+��Cl���� SO42�������ʣ��ᴿ�Ĺ����������¡�

��֪̼���Ƶ��ܽ��(S)���¶ȱ仯��������ͼ��ʾ��

�ش��������⣺
��1�������м���NaOH��ȥ������������_________________��
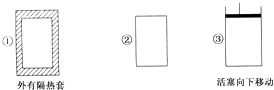
��2��ʵ���ҽ�������Ũ���ᾧ�õ�����Ҫ�����С�________���ƾ��ơ����żܵȡ�
��3�������ȹ�������Ŀ����ʹ�����ľ���ΪNa2CO3��H2O����ֹ_________________��
��4���������մ��ĸҺ�Ĵ���������________(���������)�����˹����Ѿ���ɵIJ�����������___________________________________________________��
���𰸡� Mg2+��Fe3+ ���������� ��ֹ���¶ȹ��Ͷ�����Na2CO3��7H2O��Na2CO3��10H2O���壬������ļ�����ˮ�ķѽϳ�ʱ�� ϴ�� ȡ���һ��ϴ��Һ���Թ��У��������������ữ���ټ���2��3��BaCl2��Һ������������˵����ϴ�Ӹɾ�(�����𰸺��������
��������������Ҫ�������̼�����ᴿ�������̵�������
��1��Mg2++2![]() -
-![]() Mg(OH)2����Fe3++3OH��
Mg(OH)2����Fe3++3OH��![]() Fe(OH)3���������м���NaOH��ȥ������������Mg2+��Fe3+��
Fe(OH)3���������м���NaOH��ȥ������������Mg2+��Fe3+��
��2��ʵ���ҽ�������Ũ���ᾧ�õ�����Ҫ�������������������ƾ��ơ����żܵȡ�
��3�������ȹ�������Ŀ����ʹ�����ľ���ΪNa2CO3��H2O����ֹ���¶ȹ��Ͷ�����Na2CO3��7H2O��Na2CO3��10H2O���壬������ļ�����ˮ�ķѽϳ�ʱ�䡣
��4���������մ��ĸҺ�Ĵ���������ϴ�ӣ����˹����Ѿ���ɵ�˼·�Ǽ��������Cl���� SO42�������������Ѳ�����������ѡ�����SO42����������������ȡ���һ��ϴ��Һ���Թ��У��������������ữ���ټ���2��3��BaCl2��Һ������������˵����ϴ�Ӹɾ�(�����𰸺�����ɣ���