��Ŀ����
19��x��y��z����Ԫ�ص����Ӿ�����ͬ�ĵ��Ӳ�ṹ�����Ӱ뾶x��y��y��z���γ�zy2�����ӻ������3��Ԫ�ص�ԭ��������ϵ�ǣ�������| A�� | x��y��z | B�� | y��x��z | C�� | z��x��y | D�� | z��y��x |
���� x��y��z��������Ԫ�ص����Ӿ�����ͬ�ĵ��Ӳ�ṹ�����������ӵĺ����������ȣ�y��z���γ�zy2�����ӻ������z�γ������ӣ�y�γ������ӣ���������Ų���ͬ���˵����Խ�뾶ԽС��x�����Ӱ뾶����y�����Ӱ뾶����x�γ������ӣ��ݴ��жϣ�
��� �⣺y����z�γ�zy2�͵����ӻ������z�γ������ӣ�y�γ������ӣ����Ӿ�����ͬ�ĵ��Ӳ�ṹ������Ԫ��ԭ���γ������ӵ��Ӳ���٣��γ������ӵ��Ӳ㲻�䣬����ԭ������z��y��
x�����Ӱ뾶����y�����Ӱ뾶�����Ӿ�����ͬ�ĵ��Ӳ�ṹ����x�γ������ӣ���������Ų���ͬ���˵����Խ�뾶ԽС������ԭ������y��x��
��ԭ������z��y��x��
��ѡ��D��
���� ���⿼�����뾶��С��ṹ�Ĺ�ϵ���Ѷ��еȣ���ȷ�ƶ�Ԫ�ص�λ�ù�ϵ�ǹؼ���Ҫ��ȷ��������С�ȽϹ��ɣ�

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
9����֪25�桢101kPa�����£�
��4Al��s��+3O2��g��=2Al2O3��s������H=-2834.9kJ/mol��
��4Al��s��+2O3��g��=2Al2O3��s������H=-3119.1kJ/mol���ɴ˵ó�����ȷ�����ǣ�������
��4Al��s��+3O2��g��=2Al2O3��s������H=-2834.9kJ/mol��
��4Al��s��+2O3��g��=2Al2O3��s������H=-3119.1kJ/mol���ɴ˵ó�����ȷ�����ǣ�������
| A�� | ��������O2��O3�������ͣ���O2��O3Ϊ���ȷ�Ӧ | |
| B�� | ��������O2��O3�������ߣ���O2��O3Ϊ���ȷ�Ӧ | |
| C�� | O2��O3�ȶ���3O2��g���T2O3��g����H=-284.2 kJ/mol | |
| D�� | O2��O3�ȶ���3O2��g���T2O3��g����H=+284.2 kJ/mol |
10������4Ħ����������ϡHCl��ϡNaOH��Һ��������ȫ��ת��ΪAl��OH��3������HCl��NaOH�����ʵ���֮������Ӧ�ǣ�������
| A�� | 6Ħ�� | B�� | 4Ħ�� | C�� | 16Ħ�� | D�� | 8Ħ�� |
7��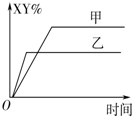 ���ܱ������У���ӦX2��g��+Y2��g��?2XY��g����H��0�ﵽ��ƽ�⣬���ı�ijһ�����ﵽ��ƽ�⣮�Դ˹��̵ķ�����ȷ���ǣ�������
���ܱ������У���ӦX2��g��+Y2��g��?2XY��g����H��0�ﵽ��ƽ�⣬���ı�ijһ�����ﵽ��ƽ�⣮�Դ˹��̵ķ�����ȷ���ǣ�������
 ���ܱ������У���ӦX2��g��+Y2��g��?2XY��g����H��0�ﵽ��ƽ�⣬���ı�ijһ�����ﵽ��ƽ�⣮�Դ˹��̵ķ�����ȷ���ǣ�������
���ܱ������У���ӦX2��g��+Y2��g��?2XY��g����H��0�ﵽ��ƽ�⣬���ı�ijһ�����ﵽ��ƽ�⣮�Դ˹��̵ķ�����ȷ���ǣ�������| A�� | �����Ǽ�С�˷�Ӧ���Ũ�ȣ���Ӧ��X2ת����һ����С | |
| B�� | �����Ǽ����˴�������Ӧ��X2�ٷֺ�����X2%�������� | |
| C�� | ��������С����������������÷�Ӧ��ƽ�ⳣ�����ֲ��� | |
| D�� | �������������¶ȣ��÷�Ӧ��ƽ�ⳣ��һ����С |
14�������������Һ������FeCl2��Һ�����ܹ۲쵽�������У�������
| A�� | �а�ɫ�������ɣ���Һ��ɫ��dz��ɫ����ɫ | |
| B�� | �к��ɫ�������ɣ��ϲ���Һ���ػ�ɫ | |
| C�� | ����ɫ��ζ�������������������ʹ�����ǵ�ľ����ȼ | |
| D�� | �ܿ�����Һ��ɫ���������������Ҳ������ų� |
4�������л���������ȷ���ǣ�������
| A�� | 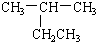 2-�һ����� 2-�һ����� | B�� | CH3CH2CH2CH2OH 1-���� | ||
| C�� |  ����ױ� ����ױ� | D�� | 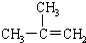 2-��-2-��ϩ 2-��-2-��ϩ |
8������˵������ȷ���ǣ�������
| A�� | ��Fe��Cu��FeCl3��Һ��ɵ�ԭ����У�������ӦʽΪ��Cu-2e-�TCu2+ | |
| B�� | ��Al��Mg��NaOH ��Һ��ɵ�ԭ����У�������ӦʽΪ��Al+4OH--3e-�TAlO2-+2H2O | |
| C�� | ��Al��Cu��ϡ������Һ��ɵ�ԭ����У�������ӦʽΪ��Cu-2e-�TCu2+ | |
| D�� | ��Al��Cu��Ũ������Һ��ɵ�ԭ����У�������ӦʽΪ��Al-3e-�TAl3+ |
9�����������϶�̼�����Ʒ�ĩ���Ƿ����̼���Ƶ�ʵ�鷽���ǣ�������
| A�� | ����ʱ��������ų� | |
| B�� | �μ�����ʱ�������ݷų� | |
| C�� | ����ˮ�μ��Ȼ�����Һ���ް�ɫ�������� | |
| D�� | ����ˮ�μӳ���ʯ��ˮ�����ް�ɫ�������� |