题目内容
关于SO2的叙述错误的是( )
| A、不能形成酸雨 |
| B、密度比空气的大 |
| C、不能与浓硫酸反应 |
| D、能使品红溶液褪色 |
考点:二氧化硫的化学性质
专题:氧族元素
分析:二氧化硫的密度大,为酸性氧化物,具有漂白性,以此来解答.
解答:
解:A.二氧化硫与水反应生成亚硫酸,再被氧化为硫酸,使雨水pH减小,可形成酸雨,故A错误;
B.其相对分子质量为64,空气的平均相对分子质量为29,可知密度比空气的大,故B正确;
C.二氧化硫与浓硫酸不能发生氧化还原反应,二者中S元素化合价分别为+4、+6,不发生归中反应,故C正确;
D.二氧化硫具有漂白性,能使品红溶液褪色,故D正确;
故选A.
B.其相对分子质量为64,空气的平均相对分子质量为29,可知密度比空气的大,故B正确;
C.二氧化硫与浓硫酸不能发生氧化还原反应,二者中S元素化合价分别为+4、+6,不发生归中反应,故C正确;
D.二氧化硫具有漂白性,能使品红溶液褪色,故D正确;
故选A.
点评:本题考查二氧化硫的性质,为高频考点,把握二氧化硫为酸性氧化物,具有漂白性为解答的关键,注意酸雨及氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有如图所示四种情况,且(2)、(3)、(4)图中分别有OA<AB,OA=AB,OA>AB,则下列分析与判断不正确的是(不计CO2的溶解)( )
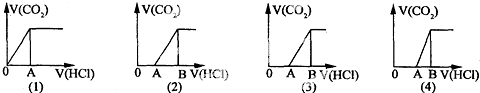

| A、M中只有一种溶质的有(1)和(3) |
| B、M中有两种溶质的有(2)和(4) |
| C、(2)图显示M中含有NaHCO3和Na2CO3两种溶质 |
| D、(4)图显示M中c(NaHCO3)>c(Na2CO3) |
元素X、Y、Z原子序数之和为33,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是( )
| A、在短周期元素中X的金属性最强 |
| B、Y的最高价含氧酸属于弱酸 |
| C、原子半径Z>Y,离子半径Z2->X+ |
| D、Y、Z都可与氢元素形成氢化物,Z的氢化物比Y的氢化物稳定 |
将如图所示实验装置的K闭合,下列判断正确的是( )
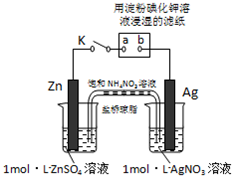

| A、Ag电极上发生氧化反应 |
| B、盐桥中NO3-向Zn电极移动 |
| C、电子沿Zn→a→b→Ag路径流动 |
| D、片刻后可观察到滤纸a点变蓝 |
将质量为w1 g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1 L.向溶液中逐渐加入浓度为a mol/L的HCl溶液,反应过程中先有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加HCl溶液体积为V2 L.将溶液蒸干灼烧得固体w2 g.下列关系式中正确的是( )
A、n(Na)+3n(Al)=
| ||
B、aV2=
| ||
| C、35.5aV2=w2-w1 | ||
| D、35.5aV2>(w2-w1) |
下列化学过程的表述或数据说明,明显不符合事实的是( )
| A、向含有1mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总的物质的量却并非是最大值 |
| B、将0.12mol Cl2通入到100mL 1mol/L的FeI2溶液中,离子方程式是:12Cl2+10Fe2++14I-→10Fe3++7I2+24Cl- |
| C、较高的温度下,可以测得0.1mol/L氨水的电离度为55%左右 |
| D、十六烷的裂化产物中不饱和烃的分子数可能会超过50% |
下列物质中,属于氧化物的是( )
| A、H3PO4 |
| B、KOH |
| C、MgO |
| D、AgNO3 |
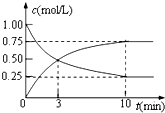 为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.(相对原子质量 C-12 H-1 O-16)
为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.(相对原子质量 C-12 H-1 O-16)