题目内容
【题目】2019年诺贝尔化学奖授予三位化学家,以表彰其对研究开发锂离子电池作出的卓越贡献。LiFePO4、聚乙二醇、LiPF6、LiAsF6和LiCl等可作锂离子聚合物电池的材料。回答下列问题:
(1)Fe的价层电子排布式为___。
(2)Li、F、P、As四种元素的电负性由大到小的顺序为___。
(3)乙二醇(HOCH2CH2OH)的相对分子质量与丙醇(CH3CH2CH2OH)相近,但沸点高出100℃,原因是___。
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
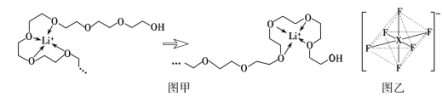
①聚乙二醇分子中,碳、氧的杂化类型分别是___、___。
②从化学键角度看,Li+迁移过程发生___(填“物理变化”或“化学变化”)。
③PF6中P的配位数为___。
④相同条件,Li+在___(填“LiPF6”或“LiAsF6”)中迁移较快,原因是___。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的品胞中所有Cl原子的分布图和原子分数坐标。据此推断该晶胞中Cl原子的数目为___。LiCl·3H2O的摩尔质量为Mg·mol-1,设NA为阿伏加德罗常数的值,则LiCl·3H2O晶体的密度为___g·cm-3(列出计算表达式)。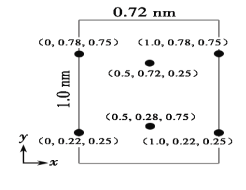
【答案】3d64s2 F、P、As、Li 乙二醇分子中羟基比丙醇的多,分子间的氢键比丙醇多,分子间作用力较大 sp3 sp3 化学变化 6 LiAsF6 AsF6-的半径比PF6-的大,AsF6-与Li+的作用力比PF6-弱 4 ![]()
【解析】
(1)Fe为26号元素,核外电子排布式为1s22s22p63s23p63d64s2;
(2)非金属性越强,电负性越强;
(3)根据氢键的数量分析判断;
(4)①根据图中聚乙二醇的碳氧键链方式分析判断杂化轨道类型;
②化学变化过程是旧键的断裂和新键的形成;
③与中心原子直接以配位键相结合的原子个数即为配位数;
④相同条件,AsF6-的半径比PF6-的大,对锂离子的作用力大小不同;
(5)根据晶胞密度公式计算;
(1)Fe为26号元素,核外电子排布式为1s22s22p63s23p63d64s2,故价层电子排布式为3d64s2;
(2)非金属性越强,电负性越强,非金属性:F>P>As>Li,则四种元素的电负性由大到小的顺序为F、P、As、Li;
(3)乙二醇分子中羟基比丙醇的多,分子间的氢键比丙醇多,分子间作用力较大;
(4)①图中聚乙二醇的碳原子都是形成4个单键,无孤电子对,为sp3杂化,氧原子都是形成2个单键,有2对孤电子,为sp3杂化;
②化学变化过程的实质是旧键的断裂和新键的形成,Li+在迁移过程中要将旧的配位键断裂,迁移后再形成新的配位键,符合化学变化过程的要求;
③与中心原子直接以配位键相结合的原子个数即为配位数,由图乙所示,PF6的中心原子为P,与之以配位键相结合的F原子有6个,则配位数为6;
④AsF6-的半径比PF6-的大,AsF6-与Li+的作用力比PF6-弱,则Li+在LiAsF6中迁移较快;
(5)如图为沿x轴投影的品胞中所有Cl原子的分布图和原子分数坐标。其中2个Cl原子在晶胞内部,4个Cl在晶胞的面上,则该晶胞中Cl原子的数目为2+4×![]() =4个;晶胞参数为0.72nm、1.0nm、0.56nm。则晶胞的体积为0.72nm×1.0nm×0.56nm=(0.72×1.0×0.56)nm3=(0.72×1.0×0.56×10-21)cm3,晶胞中含有4个Cl原子,即含有4个LiCl·3H2O,则晶胞的质量为
=4个;晶胞参数为0.72nm、1.0nm、0.56nm。则晶胞的体积为0.72nm×1.0nm×0.56nm=(0.72×1.0×0.56)nm3=(0.72×1.0×0.56×10-21)cm3,晶胞中含有4个Cl原子,即含有4个LiCl·3H2O,则晶胞的质量为![]() g,则LiCl·3H2O晶体的密度为
g,则LiCl·3H2O晶体的密度为 =
=![]() g·cm-3。
g·cm-3。