题目内容
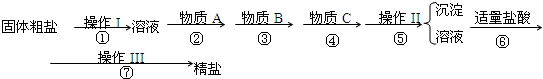
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,一位同学设计了一种制备精盐的实验方案,步骤如t图(用于生成沉淀的试剂均稍过量):
(1)判断BaCl2已过量的方法是
(2)第④步中,相关的离子方程式是
分析:由流程可知,②中加氯化钡可除去硫酸根离子,③中加NaO毫克除去镁离子,④中加碳酸钠可除去钡离子、钙离子,过滤后主要为氯化钠和碳酸钠,⑥中加盐酸反应后溶液中溶质为NaCl,然后蒸发结晶得到NaCl,以此来解答.
解答:解:由流程可知,②中加氯化钡可除去硫酸根离子,③中加NaO毫克除去镁离子,④中加碳酸钠可除去钡离子、钙离子,过滤后主要为氯化钠和碳酸钠,⑥中加盐酸反应后溶液中溶质为NaCl,然后蒸发结晶得到NaCl,
(1)BaCl2已过量,则再加氯化钡不会生成沉淀,则实验方法为用试管取少量第②步操作后的上层清液,再滴入几滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量,
故答案为:用试管取少量第②步操作后的上层清液,再滴入几滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量;
(2)④中加碳酸钠可除去钡离子、钙离子,发生离子反应为Ca2++CO32-═CaCO3↓、Ba2++CO32-═BaCO3↓,故答案为:Ca2++CO32-═CaCO3↓;Ba2++CO32-═BaCO3↓.
(1)BaCl2已过量,则再加氯化钡不会生成沉淀,则实验方法为用试管取少量第②步操作后的上层清液,再滴入几滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量,
故答案为:用试管取少量第②步操作后的上层清液,再滴入几滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量;
(2)④中加碳酸钠可除去钡离子、钙离子,发生离子反应为Ca2++CO32-═CaCO3↓、Ba2++CO32-═BaCO3↓,故答案为:Ca2++CO32-═CaCO3↓;Ba2++CO32-═BaCO3↓.
点评:本题考查物质分离、提纯实验方案的设计,把握粗盐提纯流程中的分离方法及发生的离子反应为解答的关键,侧重分析能力及物质除杂的考查,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
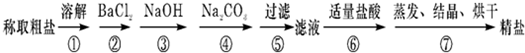
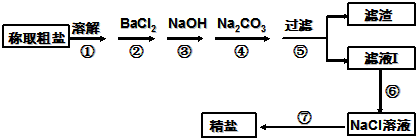
 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
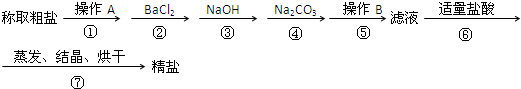
 aOH溶液 b、KOH溶液 c、BaCl2溶液 d、Ba(NO3)2溶液
aOH溶液 b、KOH溶液 c、BaCl2溶液 d、Ba(NO3)2溶液