题目内容
13.括号内两种物质的关系与概念相符的是( )| A. | 同位素(${\;}_{1}^{1}$H20与${\;}_{1}^{2}$H2O) | B. | 同素异形体(13C与C60) | ||
| C. | 同分异构体( 与CH3COOH) 与CH3COOH) | D. | 同系物(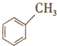 与 与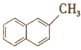 ) ) |
分析 质子数相同质量数(或中子数)不同的原子互称同位素;
同系物指结构相似、通式相同,组成上相差1个或者若干个CH2原子团,具有相同官能团的化合物;
同种元素形成的不同单质互为同素异形体;
具有相同分子式而结构不同的化合物互为同分异构体.
解答 解:A、${\;}_{1}^{1}$H20与${\;}_{1}^{2}$H2O都是水分子,属于同一物质,故A错误;
B、13C与C60一个是碳的核素、一个是碳的单质,类别不同,故B错误;
C、 与CH3COOH分子式相同,结构不同,互为同分异构体,故C正确;
与CH3COOH分子式相同,结构不同,互为同分异构体,故C正确;
D、 与
与 结构不相似,不是同系物,都属于芳香族化合物,故D错误;
结构不相似,不是同系物,都属于芳香族化合物,故D错误;
故选C.
点评 本题考查“五同”比较,难度不大,侧重考查学生的辨别能力,选项多,要细心排查,是对心理素质的考验.

练习册系列答案
相关题目
3.下列有关说法正确的是( )
| A. | 苯酚俗名石炭酸,向苯酚溶液中滴入石蕊试液溶液变浅红色 | |
| B. | 将金属钠放入乙醇中,反应较缓和且钠在液面下 | |
| C. | 既能够与酸反应又能够与碱反应的物质是两性化合物 | |
| D. | 淀粉、脂肪和纤维素都是天然高分子化合物 |
1.下列说正确的是( )
| A. | 羟基与氢氧根有相同的化学式和电子式 | |
| B. | 乙醇的官能团是-OH,乙醇是含-OH的化合物 | |
| C. | 常温下,1mol乙醇可与足量的Na反应生成11.2LH2 | |
| D. | 由工业酒精获得无水乙醇的方法是直接加热蒸馏 |
8.能用于鉴别SO2和CO2的溶液是( )
| A. | 澄清石灰水 | B. | 氯化钡溶液 | C. | 品红溶液 | D. | 紫色石蕊试液 |
18.下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是( )
| A. | 丙烷 | B. | 丙酮 | C. | 乙醛 | D. | 甲酸乙酯 |
5. 在100℃时,将0.100mol 的四氧化二氮气体充入 1L 恒容真空的密闭容器中,隔一段时间对该容器内的物质浓度进行分析得到下表数据:
在100℃时,将0.100mol 的四氧化二氮气体充入 1L 恒容真空的密闭容器中,隔一段时间对该容器内的物质浓度进行分析得到下表数据:
(1)该反应的平衡常数表达式为K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$;
从表中分析:c1<c2;c3=c4(填“>”、“<”或“=”).
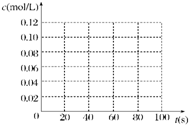
(2)在下图中画出并标明此反应中c(N2O4)和c(NO2)的浓度随时间变化的曲线.
(3)在上述条件下,从反应开始直至达到化学平衡时,四氧化二氮的平均反应速率为0.001mol/(L•s).
(4)反应达到平衡后,下列条件的改变可使NO2气体的浓度增大的是B
A.增大容器的容积 B.再充入一定量的N2O4
C.分离出一定量的NO2 D.再充入一定量的He.
 在100℃时,将0.100mol 的四氧化二氮气体充入 1L 恒容真空的密闭容器中,隔一段时间对该容器内的物质浓度进行分析得到下表数据:
在100℃时,将0.100mol 的四氧化二氮气体充入 1L 恒容真空的密闭容器中,隔一段时间对该容器内的物质浓度进行分析得到下表数据:| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)(mol/L) | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)(mol/L) | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
从表中分析:c1<c2;c3=c4(填“>”、“<”或“=”).
(2)在下图中画出并标明此反应中c(N2O4)和c(NO2)的浓度随时间变化的曲线.
(3)在上述条件下,从反应开始直至达到化学平衡时,四氧化二氮的平均反应速率为0.001mol/(L•s).
(4)反应达到平衡后,下列条件的改变可使NO2气体的浓度增大的是B
A.增大容器的容积 B.再充入一定量的N2O4
C.分离出一定量的NO2 D.再充入一定量的He.
2.下列说法中正确的是( )
| A. | 化学性质相似的有机物是同系物 | |
| B. | C3H6和C2H4一定是同系物 | |
| C. | CH3CH(CH2CH3)2和3-甲基戊烷一定是同分异构体 | |
| D. | 相对分子质量和元素及其质量分数都相同的不同分子一定是同分异构体 |
3.短周期元素W、X、Y和Z的原子序数依次增大.元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍.下列说法错误的是( )
| A. | 元素W、X的氯化物中,各原子均满足8电子的稳定结构 | |
| B. | 元素X的一种单质是自然界中硬度最大的物质 | |
| C. | 元素Y的单质只能与盐酸等酸反应生成氢气,而不能和碱反应 | |
| D. | 元素Z可与元素X形成共价化合物XZ2 |