题目内容
【题目】明矾石是制取钾肥和氢氧化铝的重要原料。明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如图所示:
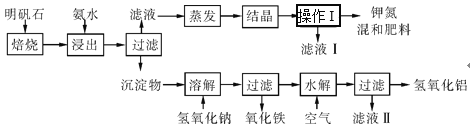
根据上述图示,完成下列填空。
(1)明矾石焙烧后用稀氨水浸出。实验需要500mL稀氨水(每升含有19.60g氨)需要取浓氨水(每升含有250.28g氨)___mL,用规格为___mL量筒量取。
(2)写出沉淀物中所有物质的化学式:___。
(3)操作Ⅰ的名称是___,所用的玻璃仪器有___。
(4)为测定混合肥料K2SO4、(NH4)2SO4中钾的含量(以K2O计),完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量BaCl2溶液,产生___。
②___、___、___(依次填写实验操作名称)。
③冷却、称重。
④若试样为mg,沉淀的物质的量为nmol,则试样中钾的含量(以K2O计)为___%(质量分数)(用含m、n的代数式表示)。
【答案】39.2 50 Al(OH)3、Al2O3、Fe2O3 过滤 漏斗、烧杯、玻璃棒 白色沉淀 过滤 洗涤 干燥 ![]()
【解析】
明矾焙烧,再加氨水,铝离子转化为氢氧化铝沉淀,过滤,滤液为硫酸铵和硫酸钾,滤渣为氢氧化铝、还含有氧化铝和少量氧化铁,滤渣中加氢氧化钠,铝的化合物转化为偏铝酸钠,氧化铁不溶解,过滤,滤液中通入空气,促进偏铝酸钠的水解生成氢氧化铝;含有硫酸铵和硫酸钾的溶液通过蒸发结晶、过滤,得到硫酸铵和硫酸钾晶体混合物,滤液中含有少量的硫酸铵和硫酸钾。
(1)配制500mL稀氨水(每升含有19.60g氨),需要使用500mL容量瓶,需要浓氨水(每升含有250.28g氨)的体积为![]() ≈0.0392L=39.2mL,所以要用50mL的量筒;
≈0.0392L=39.2mL,所以要用50mL的量筒;
(2)根据分析可知沉淀物为Al(OH)3、Al2O3、Fe2O3;
(3)操作Ⅰ之后得到滤液和滤渣,过操作Ⅰ为过滤;过滤所需要的玻璃仪器有:漏斗、烧杯、玻璃棒;
(4)①混合肥料中含有K2SO4、(NH4)2SO4,加入足量氯化钡会生成硫酸钡白色沉淀;
②本实验中需要确定生成的硫酸钡沉淀的量,从而计算出K的含量,所以要先将混合液过滤,然后洗涤沉淀,最后干燥,冷却后称重;
④设混合物中K2SO4的物质的量为x mol,(NH4)2SO4的物质的量为y mol,根据元素守恒有![]() ,解方程组可得x=
,解方程组可得x=![]() ,所以则试样中钾的含量(以K2O计)为
,所以则试样中钾的含量(以K2O计)为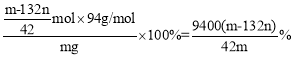 。
。

【题目】下列实验中的颜色变化,与氧化还原反应无关的是
A | B | C | D | |
实验 | 新制氯水滴入Na2S 溶液中 | 乙醇滴入K2Cr2O7酸性溶液中 | 饱和FeCl3溶液滴入沸水中 | 草酸滴入KMnO4 酸性溶液中 |
现象 | 产生黄色浑浊 | 溶液由橙色变为绿色 | 液体变为红褐色且澄清透明 | 产生无色气体,溶液紫红色褪去 |
A. AB. BC. CD. D