题目内容
2.如图为某些常见物质之间的转化关系.已知:A、B、I中含有相同的阳离子且都是XY2型化合物,I是常用的干燥剂,C为直线型分子.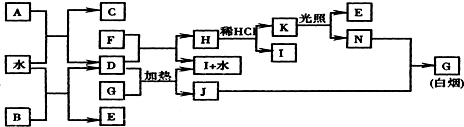
请按要求填空:
(1)B的电子式是
 ;K的结构式是H-O-Cl.
;K的结构式是H-O-Cl.(2)D与G反应的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(3)已知C的燃烧热是1300kJ/mol,表示C的燃烧热的热化学方程式是:C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol.
(4)单质F与D的反应在工业上有重要的用途,其化学方程式是2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O.
分析 解答框图推断题,要善于从题干和框图中寻找突破口,本题的比较直接的突破口有两处,一是题干中“C为直线型分子”,从框图可以看出C是A和水反应生成的,可以初步确定C是乙炔,则A为碳化钙,所以D为Ca(OH)2,B和水反应生成D和E,则B为CaO2,E为O2,N和J反应生成G是白烟,则G为NH4Cl,氢氧化钙与氯化铵加热生成氨气、氯化钙和水,所以J为NH3,I为CaCl2,则其他物质分别为:F为Cl2,H为Ca(ClO)2,K为HClO,N是HCl,据此答题.
解答 解:(1)根源以上分析,B是CaO2,是离子化合物,电子式为: ,K是次氯酸,是共价化合物,氢元素、氯元素以及氧元素均达到了稳定结构,结构式为:H-O-Cl,故答案为:
,K是次氯酸,是共价化合物,氢元素、氯元素以及氧元素均达到了稳定结构,结构式为:H-O-Cl,故答案为: ;H-O-Cl;
;H-O-Cl;
(2)根据以上分析,D为Ca(OH)2,G为NH4Cl,则D与G反应为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(3)燃烧热实指1ml可燃物燃烧生成最稳定的氧化物释放出的能量,所以乙炔燃烧的方程式为:C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol,
故答案为:C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-1300kJ/mol;
(4)F为Cl2,D为Ca(OH)2,则单质F与D的反应在工业上制漂白粉,反应方程式为:2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O,故答案为:2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O.
点评 本题是一道框图推断题,考查知识面较广,要求学生具有分析和解决问题的能力,难度较大.

 名校课堂系列答案
名校课堂系列答案| A. | Y的阳离子半径比W的阴离子半径小 | |
| B. | 气态氢化物的稳定性:X<Z<W | |
| C. | X、Z、W的氧化物对应的水化物的酸性强弱:X<Z<W | |
| D. | 室温下,含Y元素的盐形成的水溶液的pH<7 |
| A. | Fe3+、Mg2+、SO42-、Cl- | B. | Ba2+、K+、I-、NO3- | ||
| C. | Fe2+、Cu2+、AlO2-、ClO- | D. | Na+、Ca2+、Cl-、CO32- |
| A. | I2和CCl4 | B. | 乙醇和水 | C. | 汽油和苯 | D. | 水和甲苯 |
| A. | H2O2、Na2O2都属于过氧化物,都存在非极性共价键 | |
| B. | 1mol H2O2在参加反应时可能转移lmol或2mol电子 | |
| C. | H2O2在酶作用下催化分解,随着温度的升高,分解速率持续加快 | |
| D. | H2O2做漂白剂是利用其氧化性,漂白原理与HClO类似、与SO2不同 |
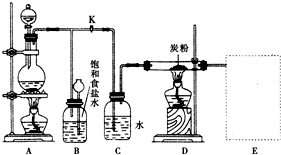 如图是一个实验室制取氯气并以氯气为原料进行特定反应的装置.
如图是一个实验室制取氯气并以氯气为原料进行特定反应的装置.