题目内容
下列叙述正确的是
- A.在电解池的阴极和原电池的负极上都发生氧化反应
- B.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
- C.用惰性电极电解KOH溶液,阴、阳两极产物的物质的量之比为1:2
- D.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH
D
试题分析:在电解池的阳极和原电池的负极上都发生氧化反应,选项A不正确;金属性是锌>铁>锡,所以镀层破损后,镀锌铁板比镀锡铁板更耐腐蚀,选项B不正确;用惰性电极电解KOH溶液,阴、阳两极产物分别是氢气和氧气,二者的物质的量之比为2:1,选项C不正确。用惰性电极电解饱和NaCl溶液的方程式是2NaCl+2H2O Cl2↑+H2↑+2NaOH,所以若有1 mol电子转移,则生成1 molNaOH,选项D正确,答案选D。
Cl2↑+H2↑+2NaOH,所以若有1 mol电子转移,则生成1 molNaOH,选项D正确,答案选D。
考点:考点原电池和电解池的有关判断、计算。该题是高考中的常见题型,属于中等难度的试题。明确原电池和电解池的工作原理,是答题的关键,有利于培养学生的逻辑推理能力和应试能力。
试题分析:在电解池的阳极和原电池的负极上都发生氧化反应,选项A不正确;金属性是锌>铁>锡,所以镀层破损后,镀锌铁板比镀锡铁板更耐腐蚀,选项B不正确;用惰性电极电解KOH溶液,阴、阳两极产物分别是氢气和氧气,二者的物质的量之比为2:1,选项C不正确。用惰性电极电解饱和NaCl溶液的方程式是2NaCl+2H2O
 Cl2↑+H2↑+2NaOH,所以若有1 mol电子转移,则生成1 molNaOH,选项D正确,答案选D。
Cl2↑+H2↑+2NaOH,所以若有1 mol电子转移,则生成1 molNaOH,选项D正确,答案选D。考点:考点原电池和电解池的有关判断、计算。该题是高考中的常见题型,属于中等难度的试题。明确原电池和电解池的工作原理,是答题的关键,有利于培养学生的逻辑推理能力和应试能力。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
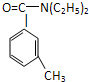 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH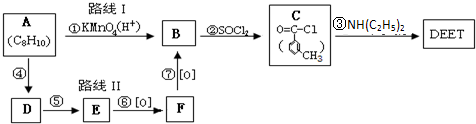
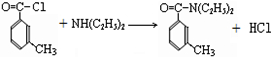
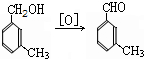
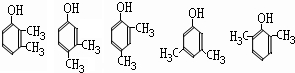 (任写2种)
(任写2种)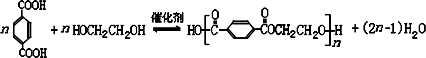
 NH3?H2O+H+
NH3?H2O+H+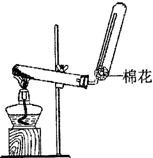 (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.