题目内容
A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素的下列叙述:
①原子半径A<B;②离子半径A>B;③原子序数A>B;④原子最外层电子数A<B;⑤A 的正价与B的负价绝对值一定相等;⑥A的电负性小于B的电负性;⑦A的第一电离能大于B的第一电离能。其中正确的组合是
| A.①②⑦ | B.③④⑥ | C.③⑤ | D.③④⑤⑥⑦ |
B
解析试题分析:A元素的阳离子和B元素的阴离子具有相同的电子层结构,则A元素处于B元素的下一周期,A为金属元素,最外层电子数较少,B为非金属元素,最外层电子数相对较多,且A的原子序数大于B,据此可以判断。①A位于B的下一周期的,且A是金属,B是非金属,所以根据同周自左向右原子半径逐渐减小可知,原子半径是A>B,①不正确;②电子层数相同的阴阳离子,离子半径随着原子序数的增大而减小,所以离子半径A<B,故②错误;③A位于B的下一周期的,且A是金属,B是非金属,所以原子序数是A>B,③正确;④A为金属元素,最外层电子数较少,B为非金属元素,最外层电子数相对较多,因此原子最外层电子数A<B,④正确;⑤A的正价和B的负价的绝对值不一定相等,如Na+和O2-,故⑤错误;⑥A是金属,B是非金属,B吸引电子的能力大于A,所以电负性A<B,故⑥正确;⑦A是金属,B是非金属,金属性越强第一电离能越小,所以第一电离能A<B,故⑦错误,答案选B。
考点:考查元素周期表的结构和元素周期律的应用

元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是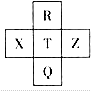
| A.非金属性:Z>T>X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R<T<Q |
| D.R、T、Q的最高正价相同 |
下列关于氢原子电子云图的说法正确的是
| A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大 |
| B.黑点密度大,单位体积内电子出现的机会大 |
| C.通常用小黑点来表示电子绕核作高速圆周运动 |
| D.电子云图是对电子运动无规律性的描述 |
2011年3月11日,日本大地震引起全世界关注,中国核事故应急协调委员会4月1曰发布,内地除西藏外都检测到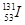 ,还检测到了极微量的人工放射性核素
,还检测到了极微量的人工放射性核素 、
、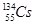 。已知铯(Cs)是钠的同族元素,据此,下列关说法正确的是( )
。已知铯(Cs)是钠的同族元素,据此,下列关说法正确的是( )
A. 、 、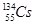 互为同位素 互为同位素 |
B.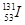 放出射线是一个自发的化学变化过程,射线对人危害很大 放出射线是一个自发的化学变化过程,射线对人危害很大 |
C.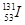 与 与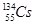 的中子数相同 的中子数相同 |
| D.单质铯的金属性比单质钠弱 |
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是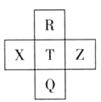
| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q |
| D.最高价氧化物的水化物的酸性: X > T |