题目内容
【题目】某兴趣小组为探究难溶性盐X(仅含三种元素)的组成和性质,设计并完成如下实验:
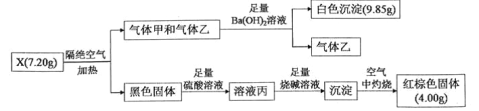
已知:气体甲和气体乙组成元素相同,物质的量之比为1:1。请回答:
(1)X的化学式为___________。
(2)溶液丙与H2O2溶液在酸性条件下反应的离子方程式是___________________________。
(3)写出利用流程图中某种物质将红棕色固体重新转化为黑色固体的化学方程式:____________。
【答案】FeC2O42Fe2++H2O2+2H+=2Fe3++2H2OFe2O3+CO![]() 2FeO+CO2
2FeO+CO2
【解析】
(1)根据流程,红棕色固体为Fe2O3,n(Fe)=![]() mol=0.05mol,甲和乙都是气体,且组成元素相同,其中气体甲能与Ba(OH)2反应生成9.85g沉淀,该沉淀是BaCO3,即n(BaCO3)=9.85/197mol=0.05mol,则n(CO)=n(CO2)=0.05mol,根据元素守恒,求出X中m(O)=(7.20-0.05×56-0.1×12)g=3.2g,即n(O)=3.2/16mol=0.2mol,n(Fe):n(C):n(O)=0.05:0.1:0.2=1:2:4,X的化学式为FeC2O4;(2)H2O2具有强氧化性,应是氧化溶液丙中的Fe2+,离子反应方程式为2Fe2++H2O2+2H+=2Fe3++2H2O;(3)FeC2O4中C显+3价,CO2中C显+4价,CO中C显+2价,且CO2和CO物质的量之比为1:1,说明Fe的价态没有发生变化,即黑色固体为FeO,因此有Fe2O3+CO
mol=0.05mol,甲和乙都是气体,且组成元素相同,其中气体甲能与Ba(OH)2反应生成9.85g沉淀,该沉淀是BaCO3,即n(BaCO3)=9.85/197mol=0.05mol,则n(CO)=n(CO2)=0.05mol,根据元素守恒,求出X中m(O)=(7.20-0.05×56-0.1×12)g=3.2g,即n(O)=3.2/16mol=0.2mol,n(Fe):n(C):n(O)=0.05:0.1:0.2=1:2:4,X的化学式为FeC2O4;(2)H2O2具有强氧化性,应是氧化溶液丙中的Fe2+,离子反应方程式为2Fe2++H2O2+2H+=2Fe3++2H2O;(3)FeC2O4中C显+3价,CO2中C显+4价,CO中C显+2价,且CO2和CO物质的量之比为1:1,说明Fe的价态没有发生变化,即黑色固体为FeO,因此有Fe2O3+CO![]() 2FeO+CO2。
2FeO+CO2。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目